ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
|
|
|
- Τιμοθέα Γεωργιάδης
- 9 χρόνια πριν
- Προβολές:
Transcript
1 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1
2 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Lucentis 10 mg/ml ενέσιμο διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα ml περιέχει 10 mg ranibizumab*. Κάθε φιαλίδιο περιέχει 2,3 mg ranibizumab σε διάλυμα 0,23 ml. *Το ranibizumab είναι ένα τμήμα ανθρωποποιημένου μονοκλωνικού αντισώματος που παράγεται από κύτταρα Escherichia coli μέσω τεχνολογίας ανασυνδυασμένου DNA. Για τον πλήρη κατάλογο των εκδόχων, βλ. παράγραφο ΦΑΡΜΑΚΟΤΕΧΝΙΚΗ ΜΟΡΦΗ Ενέσιμο διάλυμα Διαυγές, άχρωμο προς ανοικτό κίτρινο υδατικό διάλυμα. 4. ΚΛΙΝΙΚΕΣ ΠΛΗΡΟΦΟΡΙΕΣ 4.1 Θεραπευτικές ενδείξεις Το Lucentis ενδείκνυται σε ενήλικες για: Τη θεραπεία της νεοαγγειακής (υγρής μορφής) ηλικιακής εκφύλισης της ωχράς κηλίδας. Τη θεραπεία της έκπτωσης της όρασης που οφείλεται σε οίδημα της ωχράς κηλίδας διαβητικής αιτιολογίας (DME). Τη θεραπεία της έκπτωσης της όρασης που οφείλεται σε δευτεροπαθές οίδημα της ωχράς κηλίδας από απόφραξη φλέβας του αμφιβληστροειδούς (RVO κλάδου ή κεντρική RVO). Τη θεραπεία της έκπτωσης της όρασης που οφείλεται σε δευτεροπαθή χοριοειδική νεοαγγείωση (CNV) από παθολογική μυωπία (PM). 4.2 Δοσολογία και τρόπος χορήγησης Το Lucentis πρέπει να χορηγείται από οφθαλμίατρο με εμπειρία στις ενδοϋαλώδεις ενέσεις. Η συνιστώμενη δόση του Lucentis είναι 0,5 mg χορηγούμενα ως εφάπαξ ενδοϋαλώδης ένεση. Αυτό αντιστοιχεί σε όγκο ένεσης 0,05 ml. Το μεσοδιάστημα μεταξύ της χορήγησης δύο δόσεων με ένεση στον ίδιο οφθαλμό θα πρέπει να είναι τουλάχιστον τέσσερεις εβδομάδες. Η θεραπεία ξεκινά με μία ένεση ανά μήνα έως ότου επιτευχθεί μέγιστη οπτική οξύτητα και/ή δεν υπάρχουν σημεία δραστηριότητας της νόσου δηλαδή καμία μεταβολή στην οπτική οξύτητα και σε άλλα σημεία και συμπτώματα της νόσου υπό συνεχιζόμενη θεραπεία. Σε ασθενείς με υγρή μορφή AMD, DME και RVO, αρχικά μπορεί να χρειαστούν τρείς ή περισσότερες διαδοχικές μηνιαίες ενέσεις. Στη συνέχεια, η παρακολούθηση και τα μεσοδιαστήματα της θεραπείας θα πρέπει να καθορίζονται από τον γιατρό και θα πρέπει να βασίζεται στην δραστηριότητα της νόσου, όπως αυτή αξιολογείται από την οπτική οξύτητα και/ή τις ανατομικές παραμέτρους. 2
3 Εάν κατά την άποψη του γιατρού, οι οπτικές και ανατομικές παράμετροι καταδεικνύουν ότι ο ασθενής δεν ωφελείται από την συνεχιζόμενη θεραπεία, το Lucentis θα πρέπει να διακόπτεται. Η παρακολούθηση για δραστηριότητα της νόσου μπορεί να περιλαμβάνει κλινική εξέταση, ελέγχους λειτουργικότητας ή απεικονιστικές τεχνικές (π.χ. τομογραφία οπτικής πυκνότητας ή αγγειογραφία με φλουοροσεϊνη). Εάν οι ασθενείς λαμβάνουν θεραπεία σύμφωνα με το σχήμα χορήγηση θεραπείας και- παράταση, τα μεσοδιαστήματα της θεραπείας θα μπορούν σταδιακά να παραταθούν έως ότου επανεμφανιστούν σημεία δραστηριότητας της νόσου. Τα μεσοδιαστήματα της θεραπείας θα πρέπει να παρατείνονται κατά όχι περισσότερο από δύο εβδομάδες κάθε φορά για την AMD και μπορεί να παραταθούν έως ένα μήνα κάθε φορά για το DME. Για την RVO τα μεσοδιαστήματα θεραπείας μπορούν επίσης να παραταθούν σταδιακά, εντούτοις δεν υπάρχουν επαρκή δεδομένα ώστε να εξαχθούν συμπεράσματα ως προς την διάρκεια των μεσοδιατημάτων. Αν η δραστηριότητα της νόσου επανεμφανισθεί, τα μεσοδιαστήματα θα πρέπει να συντομευθούν ανάλογα. Κατά τη θεραπεία της έκπτωσης της όρασης που οφείλεται σε δευτεροπαθή χοριοειδική νεοαγγείωση (CNV) από παθολογική μυωπία (PM), πολλοί ασθενείς μπορεί να χρειαστούν μόνο μία ή δύο ενέσεις κατά το πρώτο έτος, ενώ κάποιοι ασθενείς μπορεί να χρειαστούν συχνότερη θεραπεία (βλ. παράγραφο 5.1). Lucentis και φωτοπηξία με laser στο DME και σε δευτεροπαθές οίδημα της ωχράς κηλίδας από απόφραξη κλάδου φλέβας του αμφιβληστροειδούς (BRVO) Υπάρχει κάποια εμπειρία από την χορήγηση του Lucentis ταυτόχρονα με φωτοπηξία με laser (βλ. Παράγραφο 5.1) Όταν χορηγείται την ίδια ημέρα, το Lucentis θα πρέπει να χορηγείται το λιγότερο 30 λεπτά μετά τη φωτοπηξία με laser. Το Lucentis μπορεί να χρησιμοποιηθεί σε ασθενείς που έχουν προηγουμένως υποβληθεί σε φωτοπηξία με laser. Lucentis και φωτοδυναμική θεραπεία με Visudyne σε δευτεροπαθή χοριοειδική νεοαγγείωση (CNV) από παθολογική μυωπία (PM) Δεν υπάρχει εμπειρία από την ταυτόχρονη χορήγηση Lucentis και Visudyne. Eδικοί πληθυσμοί Ηπατική δυσλειτουργία Το Lucentis δεν έχει μελετηθεί σε ασθενείς με ηπατική δυσλειτουργία. Ωστόσο, δεν απαιτείται ειδική αντιμετώπιση για το συγκεκριμένο πληθυσμό. Νεφρική δυσλειτουργία Δεν απαιτείται τροποποίηση της δόσης σε ασθενείς με νεφρική δυσλειτουργία (βλ. παράγραφο 5.2). Ηλικιωμένοι Δεν απαιτείται τροποποίηση της δόσης στους ηλικιωμένους. Υπάρχει περιορισμένη εμπειρία σε ασθενείς ηλικίας άνω των 75 ετών με DME. Παιδιατρικός πληθυσμός Η ασφάλεια και αποτελεσματικότητα του Lucentis σε παιδιά και εφήβους κάτω των 18 ετών δεν έχουν ακόμα τεκμηριωθεί. Δεν υπάρχουν διαθέσιμα δεδομένα. Τρόπος χορήγησης Φιαλίδιο μίας χρήσης αποκλειστικά για ενδοϋαλώδη χορήγηση. Το Lucentis πρέπει να ελέγχεται οπτικά για τυχόν ύπαρξη σωματιδίων και αποχρωματισμό πριν από τη χορήγηση. 3
4 Η διαδικασία της ένεσης πρέπει να πραγματοποιείται υπό άσηπτες συνθήκες, στις οποίες περιλαμβάνεται η χειρουργική αντισηψία των χεριών, η χρήση αποστειρωμένων γαντιών, αποστειρωμένου ιματίου και αποστειρωμένου διαστολέα βλεφάρων (ή ισοδύναμου), καθώς και η δυνατότητα διενέργειας αποστειρωμένης παρακέντησης (εάν χρειαστεί). Πριν από τη διενέργεια της ενδοϋαλώδους ένεσης, πρέπει να αξιολογείται προσεκτικά το ιατρικό ιστορικό του ασθενούς για αντιδράσεις υπερευαισθησίας (βλ. παράγραφο 4.4). Πριν από την ένεση, πρέπει να εφαρμόζεται κατάλληλη αναισθησία και να εφαρμόζεται ένα τοπικό μικροβιοκτόνο ευρέως φάσματος για την απολύμανση του περιοφθαλμικού δέρματος, του βλεφάρου και της οφθαλμικής επιφάνειας, σύμφωνα με την ισχύουσα τοπική πρακτική. Για πληροφορίες σχετικά με την προετοιμασία του Lucentis δείτε την παράγραφο 6.6. Η βελόνα ένεσης πρέπει να εισάγεται 3,5-4,0 mm πίσω από τη σκληροκερατοειδή στεφάνη στην υαλοειδή κοιλότητα, αποφεύγοντας τον οριζόντιο μεσημβρινό και στοχεύοντας προς το κέντρο του οφθαλμικού βολβού. Κατόπιν, χορηγείται η ποσότητα ένεσης 0,05 ml. Στις μετέπειτα ενέσεις, θα πρέπει να χρησιμοποιείται διαφορετικό σημείο του σκληρού χιτώνα. 4.3 Αντενδείξεις Υπερευαισθησία στη δραστική ουσία ή σε κάποιο από τα έκδοχα που αναφέρονται στην παράγραφο 6.1. Ασθενείς με ενεργές ή πιθανολογούμενες οφθαλμικές ή περιοφθαλμικές λοιμώξεις. Ασθενείς με ενεργή σοβαρή ενδοφθάλμια φλεγμονή. 4.4 Ειδικές προειδοποιήσεις και προφυλάξεις κατά τη χρήση Αντιδράσεις που σχετίζονται με την ενδοϋαλώδη ένεση Οι ενδοϋαλώδεις ενέσεις, στις οποίες συμπεριλαμβάνονται αυτές με το Lucentis, έχουν συνδεθεί με ενδοφθαλμίτιδα, ενδοφθάλμια φλεγμονή, ρηγματογενή αποκόλληση αμφιβληστροειδούς, ρήξη αμφιβληστροειδούς και ιατρογενή τραυματικό καταρράκτη (βλ. παράγραφο 4.8). Κατά τη χορήγηση του Lucentis, πρέπει να εφαρμόζονται πάντα κατάλληλες άσηπτες τεχνικές ένεσης. Επιπλέον, οι ασθενείς θα πρέπει να παρακολουθούνται κατά τη διάρκεια της εβδομάδας μετά την ένεση προκειμένου να επιτραπεί η έγκαιρη θεραπεία τυχόν λοίμωξης. Στους ασθενείς θα πρέπει να δίνονται οδηγίες να αναφέρουν τυχόν συμπτώματα ενδεικτικά ενδοφθαλμίτιδας ή οποιουδήποτε από τα προαναφερθέντα χωρίς καμία καθυστέρηση. Αυξήσεις της ενδοφθάλμιας πίεσης Εντός 60 λεπτών από την ένεση του Lucentis, έχουν παρατηρηθεί παροδικές αυξήσεις της ενδοφθάλμιας πίεσης (ΕΟΠ). Εμμένουσες αυξήσεις της ΕΟΠ έχουν επίσης ταυτοποιηθεί (βλ. παράγραφο 4.8). Πρέπει να παρακολουθούνται και να αντιμετωπίζονται κατάλληλα και η ενδοφθάλμια πίεση και η αιμάτωση της κεφαλής του οπτικού νεύρου. Αμφοτερόπλευρη θεραπεία Περιορισμένα δεδομένα από την αμφοτερόπλευρη χρήση του Lucentis (περιλαμβανομένης της χορήγησης την ίδια μέρα) δεν καταδεικνύουν αυξημένο κίνδυνο συστηματικών ανεπιθύμητων ενεργειών σε σύγκριση με την μονόπλευρη θεραπεία. Ανοσογονικότητα Υπάρχει πιθανότητα ανοσογονικότητας με το Lucentis. Καθώς υπάρχει η πιθανότητα αυξημένης συστηματικής έκθεσης σε ασθενείς με DME, δεν μπορεί να αποκλεισθεί ένας αυξημένος κίνδυνος ανάπτυξης υπερευαισθησίας σε αυτό τον πληθυσμό ασθενών. Θα πρέπει επίσης να δίδονται οδηγίες στους ασθενείς να αναφέρουν αν αυξάνεται η σοβαρότητα μιας ενδοφθάλμιας φλεγμονής καθώς αυτό μπορεί να αποτελεί κλινικό σημείο που να αποδίδεται στον ενδοφθάλμιο σχηματισμό αντισωμάτων. 4
5 Ταυτόχρονη χορήγηση άλλου αντι-vegf (αγγειακός ενδοθηλιακός αυξητικός παράγοντας) Το Lucentis δεν πρέπει να χορηγείται ταυτόχρονα με άλλα φαρμακευτικά προϊόντα που περιέχουν άλλους αντι-vegf (συστηματικούς ή οφθαλμικούς). Παράληψη δόσης Lucentis Η δόση θα πρέπει να παραλείπεται και η θεραπεία δεν θα πρέπει να ξαναρχίζει νωρίτερα από την επόμενη προγραμματισμένη θεραπεία σε περίπτωση: Μείωσης της καλύτερα βελτιωμένης οπτικής οξύτητας (BCVA) κατά 30 γράμματα σε σύγκριση με την τελευταία εκτίμηση της οπτικής οξύτητας Ενδοφθάλμιας πίεσης 30 mmhg Ρήξης του αμφιβληστροειδούς Υπαμφιβληστροειδικής αιμορραγίας που εμπλέκει το κέντρο του βοθρίου, ή αν το μέγεθος της αιμορραγίας είναι 50%, της συνολικής περιοχής της βλάβης Διεξαγωγής ή προγραμματισμού ενδοφθάλμιας χειρουργικής επέμβασης εντός των προηγούμενων ή επόμενων 28 ημερών. Ρήξη του μελαχρόου επιθηλίου Παράγοντες κινδύνου σχετιζόμενοι με την εμφάνιση ρήξης του μελαχρόου επιθηλίου του αμφιβληστροειδούς μετά από αντι-vegf θεραπεία για υγρή AMD, περιλαμβάνουν μεγάλη και /ή υψηλή αποκόλληση μελαχρόου επιθηλίου του αμφιβληστροειδούς. Όταν ξεκινά θεραπεία με Lucentis, θα πρέπει να δίδεται προσοχή σε ασθενείς με αυτούς του παράγοντες κινδύνου για ρήξη του μελαχρόου επιθηλίου του αμφιβληστροειδούς. Ρηγματογενής αποκόλληση αμφιβληστροειδούς ή οπές της ωχράς κηλίδας Η θεραπεία πρέπει να διακόπτεται σε ασθενείς με ρηγματογενή αποκόλληση αμφιβληστροειδούς ή οπές της ωχράς κηλίδας σταδίου 3 ή 4. Πληθυσμοί για τους οποίους υπάρχουν περιορισμένα δεδομένα Υπάρχει μόνο περιορισμένη εμπειρία στη θεραπεία ασθενών με DME που οφείλεται σε διαβήτη τύπου Ι. Το Lucentis δεν έχει μελετηθεί σε ασθενείς που έχουν προηγουμένως υποβληθεί σε θεραπεία με ενδοϋαλώδεις ενέσεις, σε ασθενείς με ενεργές συστηματικές λοιμώξεις, παραγωγική διαβητική αμφιβληστροειδοπάθεια, η σε ασθενείς με συνυπάρχουσες οφθαλμικές παθήσεις όπως η αποκόλληση του αμφιβληστροειδούς ή οπή ωχράς κηλίδας. Επίσης δεν υπάρχει εμπειρία από τη θεραπεία με Lucentis σε ασθενείς με HbA1c πάνω από 12% και μη ελεγχόμενη υπέρταση. Αυτή έλλειψη δεδομένων θα πρέπει να λαμβάνεται υπ όψη από τον ιατρό όταν υποβάλλει σε θεραπεία τέτοιους ασθενείς. Σε ασθενείς με παθολογική μυωπία, υπάρχουν περιορισμένα δεδομένα για το αποτέλεσμα του Lucentis σε ασθενείς που έχουν προηγουμένως υποβληθεί σε ανεπιτυχή φωτοδυναμική θεραπεία με verteporfin (vpdt). Επίσης, ενώ παρατηρήθηκε ένα σταθερό αποτέλεσμα σε ασθενείς με υποβοθρικές και παραβοθρικές βλάβες, δεν υπάρχουν επαρκή δεδομένα για να εξαχθούν συμπεράσματα για τη δράση του Lucentis σε ασθενείς με παθολογική μυωπία και εξωβοθριακέςβλάβες. Συστηματικές ενέργειες μετά από ενδοϋαλώδη ένεση Συστηματικές ανεπιθύμητες ενέργειες οι οποίες περιλαμβάνουν μη-οφθαλμικές αιμορραγίες και αρτηριακά θρομβοεμβολικά επεισόδια έχουν αναφερθεί μετά από ενδοϋαλώδη ένεση αναστολέων VEGF. Υπάρχουν περιορισμένα δεδομένα για την ασφάλεια στη θεραπεία ασθενών με DME, οίδημα της ωχράς κηλίδας που οφείλεται σε RVO και δευτεροπαθή CNV από PM με προηγούμενο ιστορικό εγκεφαλικού επεισοδίου ή παροδικών ισχαιμικών επεισοδίων. Πρέπει να δίδεται ιδιαίτερη προσοχή όταν αυτοί οι ασθενείς υποβάλλονται σε θεραπεία (βλ. παράγραφο 4.8). 5
6 Προηγούμενα επεισόδια RVO,ασθενών με ισχαιμική απόφραξη κλάδου φλέβας του αμφιβληστροειδούς και κεντρικής φλέβας του αμφιβληστροειδούς Υπάρχει περιορισμένη εμπειρία θεραπείας ασθενών με προηγούμενα επεισόδια RVO,ασθενών με ισχαιμική απόφραξη κλάδου φλέβας του αμφιβληστροειδούς (BRVO) και κεντρικής φλέβας του αμφιβληστροειδούς (CRVO). Σε ασθενείς στους οποίους η RVO παρουσιάζεται με κλινικά σημεία μη αναστρέψιμης ισχαιμικής απώλειας της οπτικής λειτουργίας, η θεραπεία δεν συνιστάται. 4.5 Αλληλεπιδράσεις με άλλα φαρμακευτικά προϊόντα και άλλες μορφές αλληλεπίδρασης Δεν έχουν πραγματοποιηθεί επίσημες μελέτες αλληλεπιδράσεων. Για τη συμπληρωματική χρήση φωτοδυναμικής θεραπείας (PDT) με βερτεπορφίνη και Lucentis στην υγρή AMD και την PM βλ. παράγραφο 5.1. Για τη συμπληρωματική χρήση φωτοπηξίας με laser και Lucentis στο DME και τη BRVO βλ. παραγράφους 4.2 και 5.1. Σε κλινικές μελέτες για τη θεραπεία της έκπτωσης της όρασης που οφείλεται σε DME, το αποτέλεσμα ως προς την οπτική οξύτητα ή το πάχος του κεντρικού υποπεδίου του αμφιβληστροειδούς σε ασθενείς που έλαβαν θεραπεία με Lucentis δεν επηρεάστηκε από την ταυτόχρονη θεραπεία με θειζολιδινεδιόνες. 4.6 Γονιμότητα κύηση και γαλουχία Γυναίκες σε αναπαραγωγική ηλικία/αντισύλληψη σε γυναίκες Γυναίκες σε αναπαραγωγική ηλικία πρέπει να χρησιμοποιούν αποτελεσματική αντισύλληψη κατά τη διάρκεια της θεραπείας. Εγκυμοσύνη Δεν είναι διαθέσιμα κλινικά δεδομένα από έκθεση κυήσεων για τo ranibizumab. Μελέτες σε πιθήκους cynomolgus δεν κατέδειξαν άμεση ή έμεση τοξικότητα στην εγκυμοσύνη, ή την εμβρυϊκή ανάπτυξη (βλ. παράγραφο 5.3).Η συστηματική έκθεση στο ranibizumab είναι χαμηλή μετά από οφθαλμική χορήγηση, αλλά λόγω του μηχανισμού δράσης του, το ranibizumab πρέπει να θεωρείται ότι έχει δυνητικά τερατογόνο και εμβρυοτοξική δράση. Επομένως, το ranibizumab δεν πρέπει να χρησιμοποιείται κατά τη διάρκεια της εγκυμοσύνης εκτός εάν το αναμενόμενο όφελος υπερτερεί του δυνητικού κινδύνου για το έμβρυο. Σε γυναίκες που επιθυμούν να μείνουν έγκυες και έχουν υποβληθεί σε θεραπεία με ranibizumab συνιστάται να περιμένουν το λιγότερο 3 μήνες μετά την τελευταία δόση ranibizumab πριν τη σύλληψη παιδιού. Θηλασμός Δεν είναι γνωστό εάν το Lucentis απεκκρίνεται στο ανθρώπινο γάλα. Ο θηλασμός δεν συνιστάται κατά τη διάρκεια της χρήσης του Lucentis. Γονιμότητα Δεν υπάρχουν διαθέσιμα δεδομένα για τη γονιμότητα. 4.7 Επιδράσεις στην ικανότητα οδήγησης και χειρισμού μηχανών Η διαδικασία της θεραπείας με Lucentis ενδέχεται να προκαλέσει παροδικές οπτικές διαταραχές, που μπορεί να επηρεάσουν την ικανότητα οδήγησης ή χειρισμού μηχανών (βλ. παράγραφο 4.8). Οι ασθενείς που εμφανίζουν τέτοια συμπτώματα δεν πρέπει να οδηγούν ή να χειρίζονται μηχανές έως ότου αυτές οι παροδικές οπτικές διαταραχές υποχωρήσουν. 6
7 4.8 Ανεπιθύμητες ενέργειες Σύνοψη του προφίλ ασφαλείας Η πλειονότητα των ανεπιθύμητων ενεργειών που αναφέρθηκαν μετά τη χορήγηση του Lucentis συνδέονται με την διαδικασία της ενδοϋαλώδους ένεσης. Η συχνότερα αναφερόμενες ανεπιθύμητες ενέργειες μετά την ένεση του Lucentis είναι: οφθαλμικός πόνος, οφθαλμική υπεραιμία, αυξημένη ενδοφθάλμια πίεση, φλεγμονή του υαλοειδούς σώματος, αποκόλληση του υαλοειδούς σώματος, αιμορραγία του αμφιβληστροειδούς, οπτική διαταραχή, εξιδρώματα του υαλοειδούς, αιμορραγία του επιπεφυκότα, οφθαλμικός ερεθισμός, αίσθημα ξένου σώματος στους οφθαλμούς, αυξημένη δακρύρροια, βλεφαρίτιδα, ξηροφθαλμία και οφθαλμικός κνησμός. Οι συχνότερα αναφερόμενες μη οφθαλμικές ανεπιθύμητες ενέργειες είναι πονοκέφαλος, ρινοφαρυγγίτιδα και αρθραλγία. Λιγότερο συχνά αναφερόμενες αλλά σοβαρότερες ανεπιθύμητες ενέργειες περιλαμβάνουν ενδοφθαλμίτιδα, τύφλωση, αποκόλληση αμφιβληστροειδούς, η ρήξη αμφιβληστροειδούς και ο ιατρογενής τραυματικός καταρράκτης (βλ. παράγραφο 4.4). Οι ασθενείς θα πρέπει να ενημερώνονται για τα συμπτώματα αυτών των πιθανών ανεπιθύμητων ενεργειών και να τους δίνεται οδηγία να ενημερώνουν το γιατρό τους αν αναπτύσσουν σημεία όπως οφθαλμικός πόνος ή αυξημένη δυσφορία, επιδεινούμενη ερυθρότητα του οφθαλμού, θολή ή μειωμένη όραση, έναν αυξανόμενο αριθμό μικρών σωματιδίων στην όρασή τους ή αυξημένη ευαισθησία στο φως. Οι ανεπιθύμητες ενέργειες που παρουσιάσθηκαν μετά τη χορήγηση του Lucentis σε κλινικές μελέτες συνοψίζονται στον πίνακα παρακάτω. Κατάλογος ανεπιθύμητων ενεργειών σε πίνακα # Οι ανεπιθύμητες ενέργειες παρατίθενται με ταξινόμηση κατά κατηγορία οργανικού συστήματος και συχνότητα χρησιμοποιώντας την ακόλουθη συνθήκη: πολύ συχνές ( 1/10), συχνές ( 1/100 έως <1/10), όχι συχνές ( 1/1.000 έως <1/100), σπάνιες ( 1/ έως <1/1.000), πολύ σπάνιες (<1/10.000), μη γνωστές (δεν μπορούν να εκτιμηθούν με βάση τα διαθέσιμα δεδομένα). Εντός κάθε κατηγορίας συχνότητας εμφάνισης, οι ανεπιθύμητες ενέργειες παρατίθενται κατά φθίνουσα σειρά σοβαρότητας. Λοιμώξεις και παρασιτώσεις Πολύ συχνές Συχνές Ρινοφαρυγγίτιδα Ουρολοίμωξη* Διαταραχές του αιμοποιητικού και του λεμφικού συστήματος Συχνές Αναιμία Διαταραχές του ανοσοποιητικού συστήματος Συχνές Υπερευαισθησία Ψυχιατρικές διαταραχές Συχνές Άγχος Διαταραχές του νευρικού συστήματος Πολύ συχνές Κεφαλαλγία 7
8 Οφθαλμικές διαταραχές Πολύ συχνές Συχνές Όχι συχνές Φλεγμονή του υαλοειδούς σώματος, αποκόλληση του υαλοειδούς σώματος, αιμορραγία του αμφιβληστροειδούς, οπτική διαταραχή, πόνος του οφθαλμού, εξιδρώματα του υαλοειδούς σώματος, αιμορραγία του επιπεφυκότα, ερεθισμός του οφθαλμού, αίσθηση παρουσίας ξένου σώματος στους οφθαλμούς, δακρύρροια αυξημένη, βλεφαρίτιδα, ξηροφθαλμία, υπεραιμία του οφθαλμού, κνησμός του οφθαλμού. Εκφύλιση του αμφιβληστροειδούς, διαταραχή του αμφιβληστροειδούς, αποκόλληση αμφιβληστροειδούς, ρήξη του αμφιβληστροειδούς, αποκόλληση του μελάγχρου επιθηλίου του αμφιβληστροειδούς, ρήξη του μελάγχρου επιθηλίου του αμφιβληστροειδούς, μειωμένη οπτική οξύτητα, αιμορραγία του υαλοειδούς σώματος, διαταραχή του υαλοειδούς σώματος, ραγοειδίτιδα, ιρίτιδα, ιριδοκυκλίτιδα, καταρράκτης, καταρράκτης υποκάψιος, θολερότητα του οπίσθιου περιφακίου, στικτή κερατίτιδα, εκδορά του κερατοειδούς, ερύθημα του προσθίου θαλάμου, θόλωση της όρασης, αιμορραγία στη θέση της ένεσης, αιμορραγία του οφθαλμού, επιπεφυκίτιδα, αλλεργική επιπεφυκίτιδα, οφθαλμικό έκκριμα, φωτοψία, φωτοφοβία, οφθαλμική δυσφορία, οίδημα του βλεφάρου, άλγος του βλεφάρου, υπεραιμία του επιπεφυκότα. Τύφλωση, ενδοφθαλμίτιδα, υπόπυο, ύφαιμα, κερατοπάθεια, συμφύσεις της ίριδας, εναποθέσεις του κερατοειδούς, οίδημα του κερατοειδούς γραμμώσεις του κερατοειδούς, άλγος στη θέσης ένεσης, ερεθισμός στη θέσης ένεσης, μη φυσιολογικό αίσθημα στον οφθαλμό, ερεθισμός του βλεφάρου. Διαταραχές του αναπνευστικού συστήματος,του θώρακα και του μεσοθωράκιου Συχνές βήχας Διαταραχές του γαστρεντερικού συστήματος` Συχνές Ναυτία Διαταραχές του δέρματος και του υποδόριου ιστού Συχνές Αλλεργικές αντιδράσεις (εξάνθημα, κνίδωση, κνησμός, ερύθημα) Διαταραχές του μυοσκελετικού συστήματος και του συνδετικού ιστού Πολύ συχνές Αρθραλγία Παρακλινικές εξετάσεις Πολύ συχνές Ενδοφθάλμια πίεση αυξημένη # Ως ανεπιθύμητες ενέργειες ορίστηκαν ανεπιθύμητα συμβάματα (σε τουλάχιστον 0,5 ποσοστιαίες μονάδες ασθενών) οι οποίες παρουσιάσθηκαν σε υψηλότερο ποσοστό (τουλάχιστον 2 εκατοστιαίες μονάδες) σε ασθενείς που ελάμβαναν θεραπεία με Lucentis 0,5 mg από ότι σε εκείνους που ελάμβαναν θεραπεία ελέγχου (ψευδή θεραπεία ή PDT με Verteporfin). *παρατηρήθηκε μόνο στον πληθυσμό με DME 8
9 Ανεπιθύμητες ενέργειες του προϊόντος που σχετίζονται με την κατηγορία Στις μελέτες φάσης ΙΙΙ για την υγρή AMD, η συνολική συχνότητα των μη οφθαλμικών αιμορραγιών, μιας ανεπιθύμητης ενέργειας που δυνητικά συνδέεται με τη συστηματική αναστολή του VEGF (ανθρώπινου αγγειακού ενδοθηλιακού αυξητικού παράγοντα), ήταν ελαφρά αυξημένη στους ασθενείς που υποβλήθηκαν σε θεραπεία με ranibizumab. Εν τούτοις δεν υπήρχε ακολουθία στην εμφάνιση και εξέλιξη των διαφορετικών περιστατικών αιμορραγίας. Μετά την ενδοϋαλώδη χορήγηση αναστολέων του ανθρώπινου αγγειακού ενδοθηλιακού αυξητικού παράγοντα (VEGF), υπάρχει ένας θεωρητικός κίνδυνος αρτηριακών θρομβοεμβολικών επεισοδίων, περιλαμβανομένων εγκεφαλικού επεισοδίου και εμφράγματος του μυοκαρδίου. Στις κλινικές δοκιμές του Lucentis σε ασθενείς με AMD και DME, RVO και PM παρατηρήθηκε μια χαμηλή συχνότητα εμφάνισης αρτηριακών θρομβοεμβολικών επεισοδίων, χωρίς να υπάρχουν μεγάλες διαφορές μεταξύ των ομάδων που έλαβαν θεραπεία με ranibizumab σε σύγκριση με τις ομάδες ελέγχου. Αναφορά πιθανολογούμενων ανεπιθύμητων ενεργειών Η αναφορά πιθανολογούμενων ανεπιθύμητων ενεργειών μετά από τη χορήγηση άδειας κυκλοφορίας του φαρμακευτικού προϊόντος είναι σημαντική. Επιτρέπει τη συνεχή παρακολούθηση της σχέσης οφέλους-κινδύνου του φαρμακευτικού προϊόντος. Ζητείται από τους επαγγελματίες του τομέα της υγειονομικής περίθαλψης να αναφέρουν οποιεσδήποτε πιθανολογούμενες ανεπιθύμητες ενέργειες μέσω του εθνικού συστήματος αναφοράς που αναγράφεται στο Παράρτημα V. 4.9 Υπερδοσολογία Περιστατικά τυχαίας υπερδοσολογίας έχουν αναφερθεί από τις κλινικές μελέτες στην υγρή AMD και τα δεδομένα που συλλέχθηκαν μετά την τοποθέτηση του στην αγορά. Οι ανεπιθύμητες ενέργειες που σχετίσθηκαν συχνότερα με αυτά τα περιστατικά ήταν η αύξηση της ενδοφθάλμιας πίεσης, η παροδική τύφλωση, η μειωμένη οπτική οξύτητα, το οίδημα του κερατοειδούς ο πόνος του κερατοειδούς και ο οφθαλμικός πόνος. Σε περίπτωση υπερδοσολογίας, η ενδοφθάλμια πίεση πρέπει να παρακολουθείται και να αντιμετωπίζεται καταλλήλως, εάν κρίνεται απαραίτητο από το θεράποντα ιατρό. 5. ΦΑΡΜΑΚΟΛΟΓΙΚΕΣ ΙΔΙΟΤΗΤΕΣ 5.1 Φαρμακοδυναμικές ιδιότητες Φαρμακοθεραπευτική κατηγορία: Οφθαλμολογικά, αντινεοαγγειωτικοί παράγοντες, κωδικός ATC: S01LA04 Το ranibizumab είναι ένα τμήμα ανασυνδυασμένου ανθρωποποιημένου μονοκλωνικού αντισώματος που δρα κατά του ανθρώπινου αγγειακού ενδοθηλιακού αυξητικού παράγοντα Α (VEGF-A). Συνδέεται με μεγάλη συγγένεια με τις ισομορφές του VEGF-A (π.χ. VEGF 110, VEGF 121 και VEGF 165 ), αποτρέποντας με αυτό τον τρόπο τη σύνδεση του VEGF-A με τους υποδοχείς του VEGFR- 1 και VEGFR-2. Η σύνδεση του VEGF-A με τους υποδοχείς του οδηγεί σε πολλαπλασιασμό των ενδοθηλιακών κυττάρων και νεοαγγείωση, καθώς και σε διαρροή των αγγείων. Όλα αυτά θεωρείται ότι συμβάλλουν στην εξέλιξη της νεοαγγειακής μορφής της ηλικιακής εκφύλισης της ωχράς κηλίδας, της παθολογικής μυωπίας ή της έκπτωσης της όρασης που προκαλείται είτε από οίδημα της ωχράς κηλίδας διαβητικής αιτιολογίας ή δευτεροπαθές οίδημα της ωχράς κηλίδας από RVO. Θεραπεία της υγρής AMD Στην υγρή AMD η κλινική ασφάλεια και αποτελεσματικότητα του Lucentis έχουν αξιολογηθεί σε τρεις τυχαιοποιημένες, διπλά τυφλές, ελεγχόμενες είτε με εικονική αγωγή είτε με δραστική ουσία μελέτες διάρκειας 24 μηνών σε ασθενείς με νεοαγγειακή AMD. Συνολικά ασθενείς (879 έλαβαν δραστικό φάρμακο και 444 έλαβαν φάρμακο ελέγχου) συμμετείχαν σε αυτές τις μελέτες. Στη μελέτη FVF2598g (MARINA), 716 ασθενείς με ελάχιστα κλασική ή λανθάνουσα χωρίς κλασικά στοιχεία χοριοειδική νεοαγγείωση (CNV) έλαβαν μηνιαίες ενδοϋαλώδεις ενέσεις Lucentis 0,3 mg (n=238) ή 0,5 mg (n=240), ή εικονικές ενέσεις (n=238). 9
10 Στη μελέτη FVF2587g (ANCHOR), 423 ασθενείς με αλλοιώσεις κυρίως κλασικής CNV έλαβαν είτε: 1) μηνιαίες ενδοϋαλώδεις ενέσεις Lucentis 0,3 mg και εικονική PDT (n=140), 2) μηνιαίες ενδοϋαλώδεις ενέσεις Lucentis 0,5 mg και εικονική PDT (n=140), ή 3) εικονικές ενδοϋαλώδεις ενέσεις και PDT με τη δραστική ουσία βερτεπορφίνη (n=143). Η εικονική PDT ή η PDT με τη δραστική ουσία βερτεπορφίνη χορηγήθηκαν με την αρχική ένεση Lucentis και κατόπιν κάθε 3 μήνες, εάν η αγγειογραφία με φλουορεσεΐνη έδειχνε επίμονή ή υποτροπιάζουσα διαρροή των αγγείων. Οι κύριες μετρήσεις των αποτελεσμάτων συνοψίζονται στον Πίνακα 1 και την Εικόνα 1. Πίνακας 1 Αποτελέσματα κατά το Μήνα 12 και το μήνα 24 στις μελέτες FVF2598g (MARINA) και FVF2587g (ANCHOR) Μέτρηση αποτελέσματος Απώλεια <15 γραμμάτων στον έλεγχο οπτικής οξύτητας (%) a (διατήρηση της όρασης, κύριο καταληκτικό σημείο) Κέρδος 15 γραμμάτων στον έλεγχο οπτικής οξύτητας (%) a Μέση μεταβολή οπτικής οξύτητας (γράμματα) (SD) a a p<0,01 Μήνας FVF2598g (MARINA) Εικονική Lucentis αγωγή 0,5 mg (n=238) (n=240) FVF2587g (ANCHOR) PDT με βερτεπορφίνη (n=143) Lucentis 0,5 mg (n=140) Μήνας 12 62% 95% 64% 96% Μήνας 24 53% 90% 66% 90% Μήνας 12 5% 34% 6% 40% Μήνας 24 4% 33% 6% 41% Μήνας 12-10,5 (16.6) Μήνας 24-14,9 (18,7) +7,2 (14,4) -9,5 (16,4) +11,3 (14,6) +6,6 (16,5) -9,8 (17,6) +10,7 (16,5) 10
11 Μέση μεταβολή οπτικής οξύτητας ±ΤΣ (γράμματα) Μέση μεταβολή οπτικής οξύτητας ±ΤΣ (γράμματα) Εικόνα 1 Μέση μεταβολή της οπτικής οξύτητας από την έναρξη έως το Μήνα 24 στη μελέτη FVF2598g (MARINA) και στη μελέτη FVF2587g (ANCHOR) 15 Μελέτη FVF2598g (MARINA) , , , Μήνας Μελέτη FVF2587g (ANCHOR) +10, , , Μήνας MARINA LUCENTIS 0,5 mg (n=240) Εικονική αγωγή (n=238) ANCHOR LUCENTIS 0,5 mg (n=140) PDTμε βερτεπορφίνη (n=143) Τα αποτελέσματα και από τις δύο μελέτες έδειξαν ότι η συνεχιζόμενη θεραπεία με ranibizumab μπορεί να ωφελήσει και τους ασθενείς που απώλεσαν 15 γράμματα από την καλύτερα διορθωμένη οπτική οξύτητα (BVCA) κατά τον πρώτο χρόνο θεραπείας. Η μελέτη FVF3192g (PIER) ήταν μια τυχαιοποιημένη, διπλά τυφλή, ελεγχόμενη με εικονικό φάρμακο μελέτη σχεδιασμένη να εκτιμήσει την ασφάλεια και αποτελεσματικότητα του Lucentis σε 184 ασθενείς με όλες τις μορφές της νεοαγγειακής AMD. Οι ασθενείς έλαβαν ενδοϋαλώδεις ενέσεις Lucentis 0,3 mg (n=60) ή 0,5 mg (n=61) ή εικονικές ενέσεις (n=63) μία φορά το μήνα για 3 συνεχόμενες δόσεις, ακολουθούμενες από χορήγηση μίας δόσης μία φορά κάθε 3 μήνες. Από το Μήνα 14 της μελέτης, επετράπη η διασταύρωση σε ασθενείς που υποβάλλονταν σε ψευδή θεραπεία ώστε να λάβουν ranibizumab και από τον Μήνα 19 ήταν δυνατόν να γίνονται συχνότερες θεραπείες. Οι ασθενείς που έλαβαν Lucentis στη μελέτη PIER έλαβαν κατά μέσο όρο συνολικά 10 θεραπείες. 11
12 Το κύριο καταληκτικό σημείο αποτελεσματικότητας ήταν η μέση μεταβολή της οπτικής οξύτητας στους 12 μήνες σε σύγκριση με τα αρχικά επίπεδα. Μετά από αρχική αύξηση κατά τον έλεγχο οπτικής οξύτητας (μετά από τη μηνιαία χορήγηση) κατά μέσο όρο, η οπτική οξύτητα, των ασθενών ελαττώθηκε με τριμηνιαία δόση επιστρέφοντας στην αρχική της τιμή το μήνα 12 και το αποτέλεσμα αυτό διατηρήθηκε στους περισσότερους ασθενείς που έλαβαν θεραπεία με ranibizumab (82%) τον Μήνα 24. Τα δεδομένα από ένα περιορισμένο αριθμό ασθενών που έλαβαν ranibizumab μετά από περισσότερο από ένα χρόνο ψευδούς θεραπείας υποδεικνύουν ότι η πρώιμη έναρξη της θεραπείας μπορεί να συνδέεται με καλύτερη διατήρηση της οπτικής οξύτητας. Τόσο στη μελέτη MARINA όσο και στη μελέτη ANCHOR η βελτίωση της οπτικής οξύτητας που παρατηρήθηκε με το Lucentis 0,5 mg σε 12 μήνες συνοδεύθηκε από οφέλη αναφερόμενα από τον ασθενή τα οποία μετρήθηκαν με τις τιμές του Ερωτηματολογίου για την Οπτική Λειτουργία (VFQ- 25) του National Eye Institute. Οι διαφορές μεταξύ του Lucentis 0,5 mg και των δύο ομάδων ελέγχου αξιολογήθηκαν με τις τιμές p να κυμαίνονται από 0,009 ως <0,0001. Η αποτελεσματικότητα του Lucentis στη θεραπεία της υγρής AMD έχει περεταίρω επιβεβαιωθεί σε μελέτες στην AMDπου ολοκληρώθηκαν μετά την έγκριση του προϊόντος. Δεδομένα από δύο μελέτες (MONT BLANC, BPD952A2308 και DENALI, BPD952A2309) δεν κατέδειξαν επιπρόσθετη δράση από τη συνδυασμένη χορήγηση verteporfin (Visudyne PDT) και Lucentis σε σύγκριση με τη μονοθεραπεία με Lucentis. Θεραπεία της έκπτωσης της όρασης που οφείλεται σε DME Η αποτελεσματικότητα και η ασφάλεια του Lucentis αξιολογήθηκαν σε δύο τυχαιοποιημένες, διπλά τυφλές ελεγχόμενες με εικονική ή ενεργή θεραπεία μελέτες διάρκειας 12 μηνών σε ασθενείς με έκπτωση της όρασης οφειλόμενη σε οίδημα της ωχράς κηλίδας διαβητικής αιτιολογίας. Συνολικά 496 ασθενείς (336 ενεργοί και 160 ελέγχου) συμμετείχαν σε αυτές τις μελέτες, η πλειοψηφία είχε διαβήτη τύπου ΙΙ, 28 ασθενείς που υποβλήθηκαν σε θεραπεία με ranibizumab είχαν διαβήτη τύπου Ι. Στη μελέτη φάσης ΙΙ D2201(RESOLVE). 151 ασθενείς υποβλήθηκαν σε θεραπεία με ranibizumab (6mg/ml, n=51, 10 mg/ml n=51) ή εικονική θεραπεία (n=49) με μηνιαίες ενέσεις έως ότου εκπληρωθούν τα προκαθορισμένα κριτήρια για διακοπή. Η αρχική δόση ranibizumab (0,3 mg ή 0,5 mg) μπορούσε να διπλασιασθεί σε κάθε χρονική στιγμή κατά τη διάρκεια της μελέτης μετά την πρώτη ένεση. Η φωτοπηξία με laser επιτρεπόταν ως θεραπεία διάσωσης μετά το Μήνα 3 και στα δύο σκέλη θεραπείας. Η μελέτη είχε δύο μέρη: ένα διερευνητικό μέρος (οι πρώτοι 42 ασθενείς αναλύθηκαν τον Μήνα 6) και ένα μέρος επιβεβαίωσης (οι υπόλοιποι 109 ασθενείς αναλύθηκαν το Μήνα 12). Η μεσοσταθμική μεταβολή στην BCVA από το μήνα 1 έως το μήνα 12 σε σύγκριση με τα αρχικά επίπεδα ήταν +7,8 (±7,72) γράμματα συγκεντρωτικά σε ασθενείς που έλαβαν θεραπεία με ranibizumab (n=102) και από τα δύο μέρη της μελέτης σε σύγκριση με -0,1 (±9,77) γράμματα για τους ασθενείς υπό εικονική αγωγή. (p<0,0001 για τη διαφορά της θεραπείας). Στη μελέτη φάσης ΙΙΙ D2301 (RESTORE), 345 ασθενείς με έκπτωση της όρασης που οφείλεται σε οίδημα της ωχράς κηλίδας τυχαιοποιήθηκαν ώστε να λάβουν είτε ενδοϋαλώδη ένεση με ranibizumab 0,5 mg ως μονοθεραπεία και εικονική αγωγή φωτοπηξίας με laser (n=116), συνδυασμό ranibizumab 0,5 mg και φωτοπηξία με laser photocoagulation (n=118) είτε εικονική ένεση και φωτοπηξία με laser (n=111). Η θεραπεία με ranibizumab ξεκίνησε με ενέσεις σε μηνιαία μεσοδιαστήματα και συνεχίστηκε έως ότου η οπτική οξύτητα ήταν σταθερή τουλαχιστον για τρείς συνεχόμενες μηνιαίες αξιολογήσεις. Η θεραπεία άρχισε ξανά όταν παρατηρήθηκε μείωση στην καλύτερα διορθωμένη οπτική οξύτητα (BCVA) εξαιτίας εξέλιξης του DME. Η φωτοπηξία με laser, χορηγήθηκε κατά την έναρξη την ίδια μέρα, το λιγότερο 30 λεπτά πριν από το ranibizumab, και μετά όπως ήταν αναγκαίο σύμφωνα με τα κριτήρια ΕTDRS. 12
13 Μέση μεταβολή της οπτικής οξύτητας από τα αρχικά επίπεδα +/- SE (γράμματα) 240 ασθενείς οι οποίοι είχαν προηγουμένως ολοκληρώσει τη 12μηνη μελέτη RESTORE, εντάχθηκαν στην ανοιχτή πολυκεντρική 24μηνη παράταση της μελέτη (RESTORE Extension). Οι ασθενείς έλαβαν θεραπεία με ranibizumab 0,5 mg pro re nata (PRN) στον ίδιο οφθαλμό που επιλέχθηκε ως υπό μελέτη οφθαλμός στη μελέτη D2301 (RESTORE). Η θεραπεία επαναχορηγήθηκε σε μηνιαία μεσοδιαστήματα με την εμφάνιση μείωσης στην BCVA λόγω DME και συνεχιζόταν μέχρι να επιτευχθεί σταθερή BCVA. Επιπλέον θεραπεία με laser χορηγήθηκε όταν θεωρήθηκε απαραίτητο από τον ερευνητή και με βάση τα κριτήρια ETDRS. Οι κύριες μετρήσεις των αποτελεσμάτων συνοψίζονται στον Πίνακα 2 (RESTORE και Extension) και την Εικόνα 2 (RESTORE). Εικόνα 2 Μέση μεταβολή της οπτικής οξύτητας από την έναρξη με την πάροδο του χρόνου στη μελέτη D2301 (RESTORE) ,8/+ 6, ,2/+ 5,4* , Μήνας 0 Ομάδα θεραπείας 6 Ranibizumab 0,5 mg (n=115) Ranibizumab 0,5 mg + Laser (n=118) Laser (n=110) BL=αρχικές τιμές SE=τυπικό σφάλμα από τη μέση τιμή (standard error of mean) * Διαφορές μέσων ελαχίστων τετραγώνων, p<0,0001/0,0004 βασισμένες σε αμφιπλευρη διαστρωματωμένη δοκιμασία Cochran-Mantel- Haenszel. Το αποτέλεσμα στους 12 μήνες ήταν σταθερό στις περισσότερες υποομάδες. Εντούτοις, άτομα με μια αρκετά καλή αρχική τιμή BCVA (> 73 γράμματα) μαζί με οίδημα της ωχράς κηλίδας με πάχος κεντρικού αμφιβληστροειδούς από <300 μm δεν φάνηκε να επωφελούνται από τη θεραπεία με ranibizumab σε σύγκριση με φωτοπηξία laser. 13
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Lucentis 10 mg/ml ενέσιμο διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα ml περιέχει 10 mg ranibizumab*. Κάθε
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Lucentis 10 mg/ml ενέσιμο διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα ml περιέχει 10 mg ranibizumab*. Κάθε
βλάβες στην όραση λόγω οιδήματος της ωχράς κηλίδας που προκαλείται από διαβήτη
 EMA/677928/2015 EMEA/H/C/002392 Περίληψη EPAR για το κοινό αφλιβερσέπτη Το παρόν έγγραφο αποτελεί σύνοψη της Ευρωπαϊκής Δημόσιας Έκθεσης Αξιολόγησης (EPAR) του. Επεξηγεί τον τρόπο με τον οποίο η Επιτροπή
EMA/677928/2015 EMEA/H/C/002392 Περίληψη EPAR για το κοινό αφλιβερσέπτη Το παρόν έγγραφο αποτελεί σύνοψη της Ευρωπαϊκής Δημόσιας Έκθεσης Αξιολόγησης (EPAR) του. Επεξηγεί τον τρόπο με τον οποίο η Επιτροπή
βλάβες στην όραση λόγω οιδήματος της ωχράς κηλίδας που προκαλείται από διαβήτη,
 EMA/481361/2018 EMEA/H/C/002392 Ανασκόπηση του Eylea και αιτιολογικό έγκρισης στην ΕΕ Τι είναι το Eylea και σε ποιες περιπτώσεις χρησιμοποιείται; Το Eylea είναι φάρμακο που χρησιμοποιείται για τη θεραπεία
EMA/481361/2018 EMEA/H/C/002392 Ανασκόπηση του Eylea και αιτιολογικό έγκρισης στην ΕΕ Τι είναι το Eylea και σε ποιες περιπτώσεις χρησιμοποιείται; Το Eylea είναι φάρμακο που χρησιμοποιείται για τη θεραπεία
οίδημα της ωχράς κηλίδας που οφείλεται σε απόφραξη των φλεβών πίσω από τον αμφιβληστροειδή
 EMA/491771/2014 EMEA/H/C/000715 Περίληψη EPAR για το κοινό ρανιβιζουμάμπη Το παρόν έγγραφο αποτελεί σύνοψη της Ευρωπαϊκής Δημόσιας Έκθεσης Αξιολόγησης (EPAR) του. Επεξηγεί τον τρόπο με τον οποίο η Επιτροπή
EMA/491771/2014 EMEA/H/C/000715 Περίληψη EPAR για το κοινό ρανιβιζουμάμπη Το παρόν έγγραφο αποτελεί σύνοψη της Ευρωπαϊκής Δημόσιας Έκθεσης Αξιολόγησης (EPAR) του. Επεξηγεί τον τρόπο με τον οποίο η Επιτροπή
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1.ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ URPEM monodose Ketotifen eye drops, 0.025% 0.25mg/ml οφθαλμικές σταγόνες διάλυμα σε περιέκτες μιας δόσης. 2.ΠΟΙΟΤΙΚΗ ΚΑΙ
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1.ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ URPEM monodose Ketotifen eye drops, 0.025% 0.25mg/ml οφθαλμικές σταγόνες διάλυμα σε περιέκτες μιας δόσης. 2.ΠΟΙΟΤΙΚΗ ΚΑΙ
οίδημα της ωχράς κηλίδας που οφείλεται σε απόφραξη των φλεβών πίσω από τον αμφιβληστροειδή.
 EMA/704742/2016 EMEA/H/C/000715 Περίληψη EPAR για το κοινό ρανιβιζουμάμπη Το παρόν έγγραφο αποτελεί σύνοψη της Ευρωπαϊκής Δημόσιας Έκθεσης Αξιολόγησης (EPAR) του. Επεξηγεί τον τρόπο με τον οποίο ο Οργανισμός
EMA/704742/2016 EMEA/H/C/000715 Περίληψη EPAR για το κοινό ρανιβιζουμάμπη Το παρόν έγγραφο αποτελεί σύνοψη της Ευρωπαϊκής Δημόσιας Έκθεσης Αξιολόγησης (EPAR) του. Επεξηγεί τον τρόπο με τον οποίο ο Οργανισμός
ΠΑΡΑΡΤΗΜΑ I ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΑΡΑΡΤΗΜΑ I ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 Το φάρμακο αυτό τελεί υπό συμπληρωματική παρακολούθηση. Αυτό θα επιτρέψει τον ταχύ προσδιορισμό νέων πληροφοριών ασφάλειας. Ζητείται από τους επαγγελματίες
ΠΑΡΑΡΤΗΜΑ I ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 Το φάρμακο αυτό τελεί υπό συμπληρωματική παρακολούθηση. Αυτό θα επιτρέψει τον ταχύ προσδιορισμό νέων πληροφοριών ασφάλειας. Ζητείται από τους επαγγελματίες
ΠΑΡΑΡΤΗΜΑ I ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΑΡΑΡΤΗΜΑ I ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Eylea 40 mg/ml ενέσιμο διάλυμα σε προγεμισμένη σύριγγα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα χιλιοστόλιτρο
ΠΑΡΑΡΤΗΜΑ I ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Eylea 40 mg/ml ενέσιμο διάλυμα σε προγεμισμένη σύριγγα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα χιλιοστόλιτρο
ΠΑΡΑΡΤΗΜΑ I ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΑΡΑΡΤΗΜΑ I ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Eylea 40 mg/ml ενέσιμο διάλυμα σε προγεμισμένη σύριγγα. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα χιλιοστόλιτρο
ΠΑΡΑΡΤΗΜΑ I ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Eylea 40 mg/ml ενέσιμο διάλυμα σε προγεμισμένη σύριγγα. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα χιλιοστόλιτρο
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Water for Injection/Baxter (Viaflo) 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε σάκος περιέχει 100% w/v Water for Injections.
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Water for Injection/Baxter (Viaflo) 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε σάκος περιέχει 100% w/v Water for Injections.
ΠΑΡΑΡΤΗΜΑ I ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΑΡΑΡΤΗΜΑ I ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 Το φάρμακο αυτό τελεί υπό συμπληρωματική παρακολούθηση. Αυτό θα επιτρέψει τον ταχύ προσδιορισμό νέων πληροφοριών. Ζητείται από τους επαγγελματίες
ΠΑΡΑΡΤΗΜΑ I ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 Το φάρμακο αυτό τελεί υπό συμπληρωματική παρακολούθηση. Αυτό θα επιτρέψει τον ταχύ προσδιορισμό νέων πληροφοριών. Ζητείται από τους επαγγελματίες
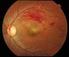
Απόφραξη φλέβας του αμφιβληστροειδούς
 Απόφραξη φλέβας του αμφιβληστροειδούς Τι είναι η απόφραξη φλέβας του αμφιβληστροειδούς; Απόφραξη φλέβας του αμφιβληστροειδούς σημαίνει ότι μία φλέβα στον αμφιβληστροειδή χιτώνα του ματιού έχει αποφραχθεί.
Απόφραξη φλέβας του αμφιβληστροειδούς Τι είναι η απόφραξη φλέβας του αμφιβληστροειδούς; Απόφραξη φλέβας του αμφιβληστροειδούς σημαίνει ότι μία φλέβα στον αμφιβληστροειδή χιτώνα του ματιού έχει αποφραχθεί.
Συν/μένα φύλλα: 18 Ο ΠΡΟΕΔΡΟΣ ΤΟΥ ΕΟΠΥΥ ΣΩΤΗΡΙΟΣ ΜΠΕΡΣΙΜΗΣ. Επ. Καθηγητής Πανεπιστημίου Πειραιώς. Μαρούσι Αρ. Πρωτ.: Γ32/ΟΙΚ.
 Μαρούσι 4-08-07 Αρ. Πρωτ.: Γ3/ΟΙΚ.356 ΓΕΝΙΚΗ Δ/ΝΣΗ: ΟΡΓΑΝΩΣΗΣ & ΣΧΕΔΙΑΣΜΟΥ ΑΓΟΡΑΣ ΥΠΗΡΕΣΙΩΝ ΥΓΕΙΑΣ Δ/ΝΣΗ: ΦΑΡΜΑΚΟΥ ΤΜΗΜA: ΣΧΕΔΙΑΣΜΟΥ ΚΑΙ ΠΑΡΑΚΟΛΟΥΘΗΣΗΣ ΧΟΡΗΓΗΣΗΣ ΦΑΡΜΑΚΩΝ Ταχ. Δ/νση: Απ. Παύλου, Μαρούσι
Μαρούσι 4-08-07 Αρ. Πρωτ.: Γ3/ΟΙΚ.356 ΓΕΝΙΚΗ Δ/ΝΣΗ: ΟΡΓΑΝΩΣΗΣ & ΣΧΕΔΙΑΣΜΟΥ ΑΓΟΡΑΣ ΥΠΗΡΕΣΙΩΝ ΥΓΕΙΑΣ Δ/ΝΣΗ: ΦΑΡΜΑΚΟΥ ΤΜΗΜA: ΣΧΕΔΙΑΣΜΟΥ ΚΑΙ ΠΑΡΑΚΟΛΟΥΘΗΣΗΣ ΧΟΡΗΓΗΣΗΣ ΦΑΡΜΑΚΩΝ Ταχ. Δ/νση: Απ. Παύλου, Μαρούσι
Version 7.2, 10/2006 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 Version 7.2, 10/2006 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Lactated Ringer s Injection/Fresenius, (3,1+0,3+6+0,2)g, ενέσιμο διάλυμα για έγχυση
Version 7.2, 10/2006 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Lactated Ringer s Injection/Fresenius, (3,1+0,3+6+0,2)g, ενέσιμο διάλυμα για έγχυση
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ERRKES. Οφθαλμικές σταγόνες, διάλυμα
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ Ketorolac Trometamol 0.5% w/v Οφθαλμικές σταγόνες, διάλυμα 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ Ketorolac Trometamol 0.5% w/v Οφθαλμικές σταγόνες, διάλυμα 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά
Τι είναι το γλαύκωμα;
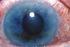 Τι είναι το γλαύκωμα; Το γλαύκωμα περιλαμβάνει μια ομάδα παθήσεων που βλάπτουν το οπτικό νεύρο, προκαλώντας διαταραχές όρασης, οι οποίες, αν δεν αντιμετωπιστούν έγκαιρα, μπορούν να εξελιχθούν και να επιφέρουν
Τι είναι το γλαύκωμα; Το γλαύκωμα περιλαμβάνει μια ομάδα παθήσεων που βλάπτουν το οπτικό νεύρο, προκαλώντας διαταραχές όρασης, οι οποίες, αν δεν αντιμετωπιστούν έγκαιρα, μπορούν να εξελιχθούν και να επιφέρουν
ΠΑΡΑΡΤΗΜΑ I ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΑΡΑΡΤΗΜΑ I ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 Το φάρμακο αυτό τελεί υπό συμπληρωματική παρακολούθηση. Αυτό θα επιτρέψει τον ταχύ προσδιορισμό νέων πληροφοριών ασφάλειας. Ζητείται από τους επαγγελματίες
ΠΑΡΑΡΤΗΜΑ I ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 Το φάρμακο αυτό τελεί υπό συμπληρωματική παρακολούθηση. Αυτό θα επιτρέψει τον ταχύ προσδιορισμό νέων πληροφοριών ασφάλειας. Ζητείται από τους επαγγελματίες
Written by Δρ Δημήτριος Ν. Γκέλης, Ιατρός, Οδοντίατρος, Ωτορινολαρυγγολόγος, -
 Πολυσακχαριδικό πολυδύναμο εμβόλιο ττνευμονιόκοκκου 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 PNEUMO 23* Ενέσιμο διάλυμα 25 mcg χ 23 / 0,5 ml P.F.Syringe (1 Dose) 1.2 Σύνθεση Δραστική ουσία: Purified
Πολυσακχαριδικό πολυδύναμο εμβόλιο ττνευμονιόκοκκου 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 PNEUMO 23* Ενέσιμο διάλυμα 25 mcg χ 23 / 0,5 ml P.F.Syringe (1 Dose) 1.2 Σύνθεση Δραστική ουσία: Purified
Οπή Ωχράς Κηλίδας. Τι είναι οπή της ωχράς;
 Οπή Ωχράς Κηλίδας Τι είναι οπή της ωχράς; Ο αμφιβληστροειδής χιτώνας είναι το φωτοευαίσθητο στρώμα ιστού που βρίσκεται στο πίσω μέρος του ματιού. Μία ειδική περιοχή του αμφιβληστροειδούς, που ονομάζεται
Οπή Ωχράς Κηλίδας Τι είναι οπή της ωχράς; Ο αμφιβληστροειδής χιτώνας είναι το φωτοευαίσθητο στρώμα ιστού που βρίσκεται στο πίσω μέρος του ματιού. Μία ειδική περιοχή του αμφιβληστροειδούς, που ονομάζεται
Παράρτημα III. Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης
 Παράρτημα III Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης Σημείωση: Οι σχετικές παράγραφοι της Περίληψης των Χαρακτηριστικών του
Παράρτημα III Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης Σημείωση: Οι σχετικές παράγραφοι της Περίληψης των Χαρακτηριστικών του
Παράρτημα III. Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης
 Παράρτημα III Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης Σημείωση: Αυτή η Περίληψη των Χαρακτηριστικών του Προϊόντος, η επισήμανση
Παράρτημα III Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης Σημείωση: Αυτή η Περίληψη των Χαρακτηριστικών του Προϊόντος, η επισήμανση
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ BACTROBAN αλοιφή 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1g αλοιφής περιέχει 20mg mupirocin. Για τον πλήρη κατάλογο
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ BACTROBAN αλοιφή 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1g αλοιφής περιέχει 20mg mupirocin. Για τον πλήρη κατάλογο
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ VAXIGRIP για παιδιά, ενέσιμο εναιώρημα σε προγεμισμένη σύριγγα. Αντιγριπικό εμβόλιο (split virion, αδρανοποιημένο). 2.
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ VAXIGRIP για παιδιά, ενέσιμο εναιώρημα σε προγεμισμένη σύριγγα. Αντιγριπικό εμβόλιο (split virion, αδρανοποιημένο). 2.
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη Eylea 40 mg/ml ενέσιμο διάλυμα σε ένα φιαλίδιο Αφλιβερσέπτη Το φάρμακο αυτό τελεί υπό συμπληρωματική παρακολούθηση. Αυτό θα επιτρέψει
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη Eylea 40 mg/ml ενέσιμο διάλυμα σε ένα φιαλίδιο Αφλιβερσέπτη Το φάρμακο αυτό τελεί υπό συμπληρωματική παρακολούθηση. Αυτό θα επιτρέψει
1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ: 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ:
 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ GLIATILIN (Choline alfoscerate) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ: GLIATILIN 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ: Μαλακές Κάψουλες:
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ GLIATILIN (Choline alfoscerate) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ: GLIATILIN 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ: Μαλακές Κάψουλες:
ΤΜΗΜΑ ΩΧΡΑΣ ΚΗΛΙ ΑΣ & ΑΜΦΙΒΛΗΣΤΡΟΕΙ ΟΥΣ ΙΑΤΡΕΙΟ ΙΑΒΗΤΙΚΗΣ ΑΜΦΙΒΛΗΣΤΡΟEI ΟΠΑΘΕΙΑΣ. ιαβήτης & Οφθαλμός
 ΤΜΗΜΑ ΩΧΡΑΣ ΚΗΛΙ ΑΣ & ΑΜΦΙΒΛΗΣΤΡΟΕΙ ΟΥΣ ΙΑΤΡΕΙΟ ΙΑΒΗΤΙΚΗΣ ΑΜΦΙΒΛΗΣΤΡΟEI ΟΠΑΘΕΙΑΣ ιαβήτης & Οφθαλμός Σακχαρώδης ιαβήτης & Όραση Ο σακχαρώδης διαβήτης είναι μία από τις κύριες αιτίες τύφλωσης στις ανεπτυγμένες
ΤΜΗΜΑ ΩΧΡΑΣ ΚΗΛΙ ΑΣ & ΑΜΦΙΒΛΗΣΤΡΟΕΙ ΟΥΣ ΙΑΤΡΕΙΟ ΙΑΒΗΤΙΚΗΣ ΑΜΦΙΒΛΗΣΤΡΟEI ΟΠΑΘΕΙΑΣ ιαβήτης & Οφθαλμός Σακχαρώδης ιαβήτης & Όραση Ο σακχαρώδης διαβήτης είναι μία από τις κύριες αιτίες τύφλωσης στις ανεπτυγμένες
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ. OXATREX, Οφθαλμικές σταγόνες, διάλυμα μιας δόσης 1,5mg/0,5ml (0,3%W/V ή 3mg/1ML)
 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ OXATREX, Οφθαλμικές σταγόνες, διάλυμα μιας δόσης 1,5mg/0,5ml (0,3%W/V ή 3mg/1ML) 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε ml
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ OXATREX, Οφθαλμικές σταγόνες, διάλυμα μιας δόσης 1,5mg/0,5ml (0,3%W/V ή 3mg/1ML) 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε ml
NeuroBloc Αλλαντική τοξίνη τύπου Β ενέσιμο διάλυμα 5.000 U/ml
 NeuroBloc Αλλαντική τοξίνη τύπου Β ενέσιμο διάλυμα 5.000 U/ml Σημαντικές πληροφορίες ασφάλειας για γιατρούς Σκοπός αυτού του εγχειριδίου είναι να παρέχει σε γιατρούς με δικαίωμα συνταγογράφησης και χορήγησης
NeuroBloc Αλλαντική τοξίνη τύπου Β ενέσιμο διάλυμα 5.000 U/ml Σημαντικές πληροφορίες ασφάλειας για γιατρούς Σκοπός αυτού του εγχειριδίου είναι να παρέχει σε γιατρούς με δικαίωμα συνταγογράφησης και χορήγησης
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ. Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο!
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο! 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία, μορφή,
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο! 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία, μορφή,
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SPC)
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SPC) 1. ΕΜΠΟΡΙΚΗ ONOMAΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DAFLON 500 mg, επικαλυμμένο με λεπτό υμένιο δισκίο. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SPC) 1. ΕΜΠΟΡΙΚΗ ONOMAΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DAFLON 500 mg, επικαλυμμένο με λεπτό υμένιο δισκίο. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ. Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο!
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο! 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία, μορφή,
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο! 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία, μορφή,
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ( SPC ) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ. 194.1μg 99μg
 1 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ( SPC ) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ VITALIPID ( ADULT ) 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1ml VITALIPID ADULT περιέχει: Δραστικά συστατικά Retinopalmitate
1 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ( SPC ) 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ VITALIPID ( ADULT ) 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1ml VITALIPID ADULT περιέχει: Δραστικά συστατικά Retinopalmitate
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ OZURDEX 700 μικρογραμμάρια ενδοϋαλώδες εμφύτευμα σε σύστημα εφαρμογής 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ OZURDEX 700 μικρογραμμάρια ενδοϋαλώδες εμφύτευμα σε σύστημα εφαρμογής 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα
SALONPAS HOT â (Capsicum extract)
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ SALONPAS HOT â (Capsicum extract) 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ SALONPAS HOT â 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε έµπλαστρο SALONPAS HOT â, µεγέθους
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ SALONPAS HOT â (Capsicum extract) 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ SALONPAS HOT â 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε έµπλαστρο SALONPAS HOT â, µεγέθους
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ. Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο!
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο! 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία, μορφή,
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο! 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία, μορφή,
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ. Hiberix, Κόνις και διαλυτικό μέσο για ενέσιμο διάλυμα Εμβόλιο έναντι του αιμόφιλου της ινφλουέντζας τύπου β (Hib)
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ Hiberix, Κόνις και διαλυτικό μέσο για ενέσιμο διάλυμα Εμβόλιο έναντι του αιμόφιλου της ινφλουέντζας τύπου β (Hib) Παρακαλούμε διαβάστε προσεκτικά αυτό το φυλλάδιο, πριν από
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ Hiberix, Κόνις και διαλυτικό μέσο για ενέσιμο διάλυμα Εμβόλιο έναντι του αιμόφιλου της ινφλουέντζας τύπου β (Hib) Παρακαλούμε διαβάστε προσεκτικά αυτό το φυλλάδιο, πριν από
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ. Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο!
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο! 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία, μορφή,
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο! 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία, μορφή,
ΠΑΡΑΡΤΗΜΑ ΙΙΙ ΤΡΟΠΟΠΟΙΗΣΗ ΣΤΙΣ ΠΕΡΙΛΗΨΕΙΣ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΚΑΙ ΣΤΟ ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 ΠΑΡΑΡΤΗΜΑ ΙΙΙ ΤΡΟΠΟΠΟΙΗΣΗ ΣΤΙΣ ΠΕΡΙΛΗΨΕΙΣ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΚΑΙ ΣΤΟ ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ Αυτές οι μεταβολές στη ΠΧΠ και το φύλλο οδηγιών χρήσης θα είναι εν ισχύ κατά την έκδοση της Κοινοτικής
ΠΑΡΑΡΤΗΜΑ ΙΙΙ ΤΡΟΠΟΠΟΙΗΣΗ ΣΤΙΣ ΠΕΡΙΛΗΨΕΙΣ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΚΑΙ ΣΤΟ ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ Αυτές οι μεταβολές στη ΠΧΠ και το φύλλο οδηγιών χρήσης θα είναι εν ισχύ κατά την έκδοση της Κοινοτικής
ΔΙΑΒΗΤΙΚΗ ΑΜΦΙΒΛΗΣΤΡΟΕΙΔΟΠΑΘΕΙΑ
 ΔΙΑΒΗΤΙΚΗ ΑΜΦΙΒΛΗΣΤΡΟΕΙΔΟΠΑΘΕΙΑ Ένας ενημερωτικός οδηγός για την πραγματικότητα του σήμερα Δρ. Αναστάσιος Ιωάννης Κανελλόπουλος Καθηγητής Οφθαλμολογίας Παν/μιου Νέας Υόρκης Οφθαλμολογικό Ινστιτούτο Laser
ΔΙΑΒΗΤΙΚΗ ΑΜΦΙΒΛΗΣΤΡΟΕΙΔΟΠΑΘΕΙΑ Ένας ενημερωτικός οδηγός για την πραγματικότητα του σήμερα Δρ. Αναστάσιος Ιωάννης Κανελλόπουλος Καθηγητής Οφθαλμολογίας Παν/μιου Νέας Υόρκης Οφθαλμολογικό Ινστιτούτο Laser
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1/5 1. ΕΜΠΟΡΙΚΗ ONOMAΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DAFLON 500 mg, επικαλυμμένο με λεπτό υμένιο δισκίο. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1/5 1. ΕΜΠΟΡΙΚΗ ONOMAΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DAFLON 500 mg, επικαλυμμένο με λεπτό υμένιο δισκίο. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ
Written by Δρ Δημήτριος Ν. Γκέλης, Ιατρός, Οδοντίατρος, Ωτορινολαρυγγολόγος, -
 TOBREX 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία: Τ Ο Β R Ε Χ Οφθαλμικές σταγόνες, διάλυμα 0,3% 1.2 Σύνθεση: Δραστική ουσία: Tobramycin (Τομπραμυκίνη) Έκδοχα: Benzalkonium chloride, Boric acid,
TOBREX 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία: Τ Ο Β R Ε Χ Οφθαλμικές σταγόνες, διάλυμα 0,3% 1.2 Σύνθεση: Δραστική ουσία: Tobramycin (Τομπραμυκίνη) Έκδοχα: Benzalkonium chloride, Boric acid,
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Cetrotide 0,25 mg κόνις και διαλύτης για ενέσιμο διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φιαλίδιο περιέχει 0,25
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Cetrotide 0,25 mg κόνις και διαλύτης για ενέσιμο διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φιαλίδιο περιέχει 0,25
Παράρτημα III. Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης
 Παράρτημα III Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης Σημείωση: Αυτή η Περίληψη των Χαρακτηριστικών του Προϊόντος, η επισήμανση
Παράρτημα III Τροποποιήσεις των σχετικών παραγράφων της περίληψης των χαρακτηριστικών του προϊόντος και των φύλλων οδηγιών χρήσης Σημείωση: Αυτή η Περίληψη των Χαρακτηριστικών του Προϊόντος, η επισήμανση
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη. Eylea 40 mg/ml ενέσιμο διάλυμα σε ένα φιαλίδιο Αφλιβερσέπτη
 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη Eylea 40 mg/ml ενέσιμο διάλυμα σε ένα φιαλίδιο Αφλιβερσέπτη Το φάρμακο αυτό τελεί υπό συμπληρωματική παρακολούθηση. Αυτό θα επιτρέψει τον ταχύ προσδιορισμό
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη Eylea 40 mg/ml ενέσιμο διάλυμα σε ένα φιαλίδιο Αφλιβερσέπτη Το φάρμακο αυτό τελεί υπό συμπληρωματική παρακολούθηση. Αυτό θα επιτρέψει τον ταχύ προσδιορισμό
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ SEPTANEST 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Αρτικαΐνη υδροχλωρική 4% με επινεφρίνη 1:200000 ARTICAINE HYDROCHLORIDE & EPINEPHRINE
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ SEPTANEST 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Αρτικαΐνη υδροχλωρική 4% με επινεφρίνη 1:200000 ARTICAINE HYDROCHLORIDE & EPINEPHRINE
ΠΑΡΑΡΤΗΜΑ I ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΑΡΑΡΤΗΜΑ I ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 Το φάρμακο αυτό τελεί υπό συμπληρωματική παρακολούθηση. Αυτό θα επιτρέψει τον γρήγορο προσδιορισμό νέων πληροφοριών ασφάλειας. Ζητείται από τους
ΠΑΡΑΡΤΗΜΑ I ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 Το φάρμακο αυτό τελεί υπό συμπληρωματική παρακολούθηση. Αυτό θα επιτρέψει τον γρήγορο προσδιορισμό νέων πληροφοριών ασφάλειας. Ζητείται από τους
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DYNAPEN 3
 ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DYNAPEN 3 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά FISH OIL (EICOSAPENTAENOIC ACID) & (DOCOSAHEXAENOIC
ΠΕΡΙΛΗΨΗ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ DYNAPEN 3 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ σε δραστικά συστατικά FISH OIL (EICOSAPENTAENOIC ACID) & (DOCOSAHEXAENOIC
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ EVATON Β 12 Επικαλυμένα με λεπτό υμένιο δισκία (200+250+1.5) mg
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ EVATON Β 12 Επικαλυμένα με λεπτό υμένιο δισκία (200+250+1.5) mg 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ: EVATON B 12 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ :
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ EVATON Β 12 Επικαλυμένα με λεπτό υμένιο δισκία (200+250+1.5) mg 1. ΕΜΠΟΡΙΚΗ ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ: EVATON B 12 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ :
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Aflen 300 mg καψάκια σκληρά Triflusal Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο,
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Aflen 300 mg καψάκια σκληρά Triflusal Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο,
Τι είναι η ωχρά κηλίδα;
 Τι είναι η ωχρά κηλίδα; Η ωχρά κηλίδα είναι το κεντρικό τμήμα του αμφιβληστροειδή, ένα λεπτό στρώμα φωτοευαίσθητων νευρικών κυττάρων και ινών που βρίσκεται στο πίσω μέρος του οφθαλμού. Ο αμφιβληστροειδής
Τι είναι η ωχρά κηλίδα; Η ωχρά κηλίδα είναι το κεντρικό τμήμα του αμφιβληστροειδή, ένα λεπτό στρώμα φωτοευαίσθητων νευρικών κυττάρων και ινών που βρίσκεται στο πίσω μέρος του οφθαλμού. Ο αμφιβληστροειδής
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΕΩΣ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΕΩΣ Covexin 10, ενέσιμο εναιώρημα για πρόβατα και βοοειδή 1. ΟΝΟΜΑ ΚΑΙ ΔΙΕΥΘΥΝΣΗ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ ΚΑΙ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΠΑΡΑΓΩΓΗΣ ΠΟΥ ΕΙΝΑΙ ΥΠΕΥΘΥΝΟΣ ΓΙΑ ΤΗΝ ΑΠΟΔΕΣΜΕΥΣΗ
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΕΩΣ Covexin 10, ενέσιμο εναιώρημα για πρόβατα και βοοειδή 1. ΟΝΟΜΑ ΚΑΙ ΔΙΕΥΘΥΝΣΗ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ ΚΑΙ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΠΑΡΑΓΩΓΗΣ ΠΟΥ ΕΙΝΑΙ ΥΠΕΥΘΥΝΟΣ ΓΙΑ ΤΗΝ ΑΠΟΔΕΣΜΕΥΣΗ
Β Οφθαλμολογική Κλινική Α.Π.Θ. ΣΤΟΙΧΕΙΩΔΕΙΣ ΔΕΞΙΟΤΗΤΕΣ ΣΤΗΝ ΟΦΘΑΛΜΟΛΟΓΙΑ IΙ (9-19) Εκδοχή 7/1.10.11
 Β Οφθαλμολογική Κλινική Α.Π.Θ. ΣΤΟΙΧΕΙΩΔΕΙΣ ΔΕΞΙΟΤΗΤΕΣ ΣΤΗΝ ΟΦΘΑΛΜΟΛΟΓΙΑ IΙ (9-19) Εκδοχή 7/1.10.11 11 Θεωρητικές Δεξιότητες Πόνος Διαταραχές οπτικής λειτουργίας 9. Επιφανειακός Πόνος 10. Ασθενωπία Διόφθαλμή
Β Οφθαλμολογική Κλινική Α.Π.Θ. ΣΤΟΙΧΕΙΩΔΕΙΣ ΔΕΞΙΟΤΗΤΕΣ ΣΤΗΝ ΟΦΘΑΛΜΟΛΟΓΙΑ IΙ (9-19) Εκδοχή 7/1.10.11 11 Θεωρητικές Δεξιότητες Πόνος Διαταραχές οπτικής λειτουργίας 9. Επιφανειακός Πόνος 10. Ασθενωπία Διόφθαλμή
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ECTOPOR 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ
 ECTOPOR 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ ECTOPOR 2. Ποιοτική και Ποσοτική σύνθεση Δραστικό συστατικό Cypermethrin high cis 2% (w/v) Έκδοχα Βλ. πλήρη κατάλογο εκδόχων στο κεφάλαιο 6.1.
ECTOPOR 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ ECTOPOR 2. Ποιοτική και Ποσοτική σύνθεση Δραστικό συστατικό Cypermethrin high cis 2% (w/v) Έκδοχα Βλ. πλήρη κατάλογο εκδόχων στο κεφάλαιο 6.1.
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ Fortrans 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ FORTRANS, σκόνη για πόσιμο διάλυμα σε φακελλίσκους. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φακελλίσκος περιέχει:
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ Fortrans 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ FORTRANS, σκόνη για πόσιμο διάλυμα σε φακελλίσκους. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φακελλίσκος περιέχει:
Terbinafine/Target Terbinafine hydrochloride
 Terbinafine/Target Terbinafine hydrochloride ΦΥΛΛΟ Ο ΗΓΙΩΝ ΧΡΗΣΗΣ 1. ΠΡΟΣ ΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονοµασία ιδιοσκευάσµατος Τerbinafine/Target δερµατικό εκνέφωµα, διάλυµα 1%. 1.2 Σύνθεση
Terbinafine/Target Terbinafine hydrochloride ΦΥΛΛΟ Ο ΗΓΙΩΝ ΧΡΗΣΗΣ 1. ΠΡΟΣ ΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονοµασία ιδιοσκευάσµατος Τerbinafine/Target δερµατικό εκνέφωµα, διάλυµα 1%. 1.2 Σύνθεση
FLORKEM 300 mg/ml ενέσιµο διάλυµα για βοοειδή και χοίρους
 FLORKEM 300 mg/ml ενέσιµο διάλυµα για βοοειδή και χοίρους ΣΥΝΘΕΣΗ 1 ml περιέχει: Florfenicol.300 mg Ωχρο-κίτρινο έως διαυγές κίτρινο διάλυµα. ΕΝ ΕΙΞΕΙΣ Λοιµώξεις που οφείλονται σε βακτήρια ευαίσθητα στη
FLORKEM 300 mg/ml ενέσιµο διάλυµα για βοοειδή και χοίρους ΣΥΝΘΕΣΗ 1 ml περιέχει: Florfenicol.300 mg Ωχρο-κίτρινο έως διαυγές κίτρινο διάλυµα. ΕΝ ΕΙΞΕΙΣ Λοιµώξεις που οφείλονται σε βακτήρια ευαίσθητα στη
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤOY ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤOY ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Influvac sub-unit, ενέσιμο εναιώρημα (αντιγριπικό εμβόλιο, απενεργοποιημένων επιφανειακών αντιγόνων). 2. ΠΟΙΟΤΙΚΗ ΚΑΙ
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤOY ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Influvac sub-unit, ενέσιμο εναιώρημα (αντιγριπικό εμβόλιο, απενεργοποιημένων επιφανειακών αντιγόνων). 2. ΠΟΙΟΤΙΚΗ ΚΑΙ
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ NEVANAC 1 mg/ml οφθαλμικές σταγόνες, εναιώρημα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1 ml εναιωρήματος περιέχει
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ NEVANAC 1 mg/ml οφθαλμικές σταγόνες, εναιώρημα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1 ml εναιωρήματος περιέχει
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ PULVO 47, αερόλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα γραμμάριο PULVO 47 περιέχει 2,70 mg (10811 UC*) horse liver catalase
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ PULVO 47, αερόλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα γραμμάριο PULVO 47 περιέχει 2,70 mg (10811 UC*) horse liver catalase
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ. Λιδοκαΐνη Υδροχλωρική Μονοϋδρική 2%+ επινεφρίνη 1:80000Τοπικό αναισθητικό + επινεφρίνη ή νορεπινεφρίνη
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ LIGNOSPAN 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Λιδοκαΐνη Υδροχλωρική Μονοϋδρική 2%+ επινεφρίνη 1:80000Τοπικό αναισθητικό +
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ LIGNOSPAN 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Λιδοκαΐνη Υδροχλωρική Μονοϋδρική 2%+ επινεφρίνη 1:80000Τοπικό αναισθητικό +
Το Stelara είναι φάρμακο που χρησιμοποιείται για τη θεραπεία των ακόλουθων παθήσεων:
 EMA/636854/2016 EMEA/H/C/000958 Περίληψη EPAR για το κοινό ουστεκινουμάμπη Το παρόν έγγραφο αποτελεί σύνοψη της Ευρωπαϊκής Δημόσιας Έκθεσης Αξιολόγησης (EPAR) του. Επεξηγεί τον τρόπο με τον οποίο ο Οργανισμός
EMA/636854/2016 EMEA/H/C/000958 Περίληψη EPAR για το κοινό ουστεκινουμάμπη Το παρόν έγγραφο αποτελεί σύνοψη της Ευρωπαϊκής Δημόσιας Έκθεσης Αξιολόγησης (EPAR) του. Επεξηγεί τον τρόπο με τον οποίο ο Οργανισμός
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ AIR SALONPAS 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Τα 100 ml του αερολύµατος για τοπική χρήση περιέχουν: Methyl salicylate 1.75g
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ AIR SALONPAS 2. ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Τα 100 ml του αερολύµατος για τοπική χρήση περιέχουν: Methyl salicylate 1.75g
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη CromoHEXAL eye drops Νατριούχος Χρωμογλυκίνη
 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη CromoHEXAL eye drops Νατριούχος Χρωμογλυκίνη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης πριν αρχίσετε να χρησιμοποιείτε αυτό το φάρμακο, διότι
Φύλλο οδηγιών χρήσης: Πληροφορίες για τον χρήστη CromoHEXAL eye drops Νατριούχος Χρωμογλυκίνη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης πριν αρχίσετε να χρησιμοποιείτε αυτό το φάρμακο, διότι
1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ Versifel FeLV ενέσιμο εναιώρημα για γάτες
 ΠΑΡΑΡΤΗΜΑ 1: ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ Versifel FeLV ενέσιμο εναιώρημα για γάτες 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε δόση 1ml περιέχει:
ΠΑΡΑΡΤΗΜΑ 1: ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ Versifel FeLV ενέσιμο εναιώρημα για γάτες 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε δόση 1ml περιέχει:
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SPC)
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SPC) ΑΝΘΡΩΠΙΝΗ, ΑΝΤΙΤΕΤΑΝΙΚΗ ΑΝΟΣΟΣΦΑΙΡΙΝΗ Ε.Μ. (HUMAN TETANUS IMMUNOGLOBULIN, I.M.) 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ TETAGAM P 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ (SPC) ΑΝΘΡΩΠΙΝΗ, ΑΝΤΙΤΕΤΑΝΙΚΗ ΑΝΟΣΟΣΦΑΙΡΙΝΗ Ε.Μ. (HUMAN TETANUS IMMUNOGLOBULIN, I.M.) 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ TETAGAM P 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Molaxole κόνις για πόσιμο διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φακελλίσκος περιέχει τις ακόλουθες δραστικές ουσίες:
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Molaxole κόνις για πόσιμο διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φακελλίσκος περιέχει τις ακόλουθες δραστικές ουσίες:
1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ. Metacam 5 mg/ml ενέσιμο διάλυμα για βοοειδή και χοίρους 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ
 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Metacam 5 mg/ml ενέσιμο διάλυμα για βοοειδή και χοίρους 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα ml περιέχει: Δραστικό συστατικό: Μελοξικάμη 5 mg Έκδοχο:
1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Metacam 5 mg/ml ενέσιμο διάλυμα για βοοειδή και χοίρους 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Ένα ml περιέχει: Δραστικό συστατικό: Μελοξικάμη 5 mg Έκδοχο:
Φύλλο οδηγιών για το χρήστη. Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο!
 Φύλλο οδηγιών για το χρήστη Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο! 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία, μορφή, περιεκτικότητα T r a
Φύλλο οδηγιών για το χρήστη Οδηγίες για τον ασθενή - παρακαλούμε διαβάστε προσεκτικά πριν πάρετε αυτό το φάρμακο! 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία, μορφή, περιεκτικότητα T r a
B. ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 B. ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 29 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον ασθενή Parsabiv 2,5 mg ενέσιμο διάλυμα Parsabiv 5 mg ενέσιμο διάλυμα Parsabiv 10 mg ενέσιμο διάλυμα etelcalcetide Το φάρμακο αυτό τελεί
B. ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 29 Φύλλο οδηγιών χρήσης: Πληροφορίες για τον ασθενή Parsabiv 2,5 mg ενέσιμο διάλυμα Parsabiv 5 mg ενέσιμο διάλυμα Parsabiv 10 mg ενέσιμο διάλυμα etelcalcetide Το φάρμακο αυτό τελεί
ΓΛΑΥΚΩΜΑ. προληψη και θεραπεια. επειδή είναι σηµαντικό να διατηρήσετε για πάντα την όραση σας
 ΓΛΑΥΚΩΜΑ προληψη και θεραπεια επειδή είναι σηµαντικό να διατηρήσετε για πάντα την όραση σας Τι είναι το γλαύκωµα; Το γλαύκωμα αποτελεί μια ομάδα από παθήσεις των οφθαλμών, οι οποίες έχουν σαν κοινό χαρακτηριστικό
ΓΛΑΥΚΩΜΑ προληψη και θεραπεια επειδή είναι σηµαντικό να διατηρήσετε για πάντα την όραση σας Τι είναι το γλαύκωµα; Το γλαύκωμα αποτελεί μια ομάδα από παθήσεις των οφθαλμών, οι οποίες έχουν σαν κοινό χαρακτηριστικό
Written by Δρ Δημήτριος Ν. Γκέλης, Ιατρός, Οδοντίατρος, Ωτορινολαρυγγολόγος, Wednesday, 19 December :05 -
 SUPERAMIN ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ 1.1 Ονομασία Προϊόντος: SUPERAMIN α) Πόσιμο διάλυμα σε συσκευασία μιας δόσης 1 g/10ml FL & g/10ml FL β) Ενέσιμο διάλυμα 1 g/5ml AMP & 2g/5ml AMP 1.2 Σύνθεση: Δραστική
SUPERAMIN ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ 1.1 Ονομασία Προϊόντος: SUPERAMIN α) Πόσιμο διάλυμα σε συσκευασία μιας δόσης 1 g/10ml FL & g/10ml FL β) Ενέσιμο διάλυμα 1 g/5ml AMP & 2g/5ml AMP 1.2 Σύνθεση: Δραστική
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ PEVARYL Kρέμα 1% w/w Νιτρική εκοναζόλη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να χρησιμοποιείτε αυτό
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ PEVARYL Kρέμα 1% w/w Νιτρική εκοναζόλη Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να χρησιμοποιείτε αυτό
Παράρτημα III. Τροποποιήσεις στις σχετικές παραγράφους των πληροφοριών προϊόντος
 Παράρτημα III Τροποποιήσεις στις σχετικές παραγράφους των πληροφοριών προϊόντος Σημείωση: Οι αλλαγές στις σχετικές παραγράφους της Περίληψης των Χαρακτηριστικών Προϊόντος και του Φύλλου Οδηγιών Χρήσης
Παράρτημα III Τροποποιήσεις στις σχετικές παραγράφους των πληροφοριών προϊόντος Σημείωση: Οι αλλαγές στις σχετικές παραγράφους της Περίληψης των Χαρακτηριστικών Προϊόντος και του Φύλλου Οδηγιών Χρήσης
1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ. CANIGEN DHPPi λυοφιλοποιημένο υλικό και διαλύτης για παρασκευή ενέσιμου εναιωρήματος για σκύλους
 ΠΑΡΑΡΤΗΜΑ 1: ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ CANIGEN DHPPi λυοφιλοποιημένο υλικό και διαλύτης για παρασκευή ενέσιμου εναιωρήματος για σκύλους
ΠΑΡΑΡΤΗΜΑ 1: ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ CANIGEN DHPPi λυοφιλοποιημένο υλικό και διαλύτης για παρασκευή ενέσιμου εναιωρήματος για σκύλους
Γλαύκωμα: H σιωπηλή ασθένεια τύφλωσης
 Γλαύκωμα: H σιωπηλή ασθένεια τύφλωσης Οι παράγοντες επικινδυνότητας για τη δημιουργία γλαυκώματος είναι: Το Γλαύκωμα είναι μια ομάδα οφθαλμικών παθήσεων που προξενεί προοδευτική βλάβη στο οπτικό νεύρο,
Γλαύκωμα: H σιωπηλή ασθένεια τύφλωσης Οι παράγοντες επικινδυνότητας για τη δημιουργία γλαυκώματος είναι: Το Γλαύκωμα είναι μια ομάδα οφθαλμικών παθήσεων που προξενεί προοδευτική βλάβη στο οπτικό νεύρο,
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ TOBREX Οφθαλµική αλοιφή 0,3% 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1 g αλοιφής περιέχει 3 mg τοµπραµυκίνης. Για τα έκδοχα,
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ TOBREX Οφθαλµική αλοιφή 0,3% 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ 1 g αλοιφής περιέχει 3 mg τοµπραµυκίνης. Για τα έκδοχα,
2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ. Κάθε ml διαλύματος περιέχει Sodium Diclofenac 1mg + Tobramycin 3mg
 TOBRAFEN Diclofenac Sodium 0.1% + Tobramycin 0.3% 1. ΟΝΟΜΑ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ TOBRAFEN Οφθαλμικές Σταγόνες, Διάλυμα 0,1%+0,3% 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ Κάθε ml διαλύματος
TOBRAFEN Diclofenac Sodium 0.1% + Tobramycin 0.3% 1. ΟΝΟΜΑ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ TOBRAFEN Οφθαλμικές Σταγόνες, Διάλυμα 0,1%+0,3% 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ Κάθε ml διαλύματος
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ BTVPUR AlSap 4, ενέσιµο εναιώρηµα για πρόβατα. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε δόση του
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ BTVPUR AlSap 4, ενέσιµο εναιώρηµα για πρόβατα. 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε δόση του
ασθενών με σοβαρή, ενεργό νόσο που δεν έχουν προηγουμένως λάβει θεραπευτική αγωγή με μεθοτρεξάτη,
 EMA/502328/2014 EMEA/H/C/000955 Περίληψη EPAR για το κοινό τοκιλιζουμάμπη Το παρόν έγγραφο αποτελεί σύνοψη της Ευρωπαϊκής Δημόσιας Έκθεσης Αξιολόγησης (EPAR) του. Επεξηγεί τον τρόπο με τον οποίο η Επιτροπή
EMA/502328/2014 EMEA/H/C/000955 Περίληψη EPAR για το κοινό τοκιλιζουμάμπη Το παρόν έγγραφο αποτελεί σύνοψη της Ευρωπαϊκής Δημόσιας Έκθεσης Αξιολόγησης (EPAR) του. Επεξηγεί τον τρόπο με τον οποίο η Επιτροπή
ΟΔΗΓΟΣ ΓΙΑ ΝΑ ΑΡΧΙΣΕΤΕ ΜΕ ΤΟ APIDRA ενέσιμο διάλυμα σε φιαλίδιο των 10 ml
 Rev 02 - Final ΟΔΗΓΟΣ ΓΙΑ ΝΑ ΑΡΧΙΣΕΤΕ ΜΕ ΤΟ APIDRA ενέσιμο διάλυμα σε φιαλίδιο των 10 ml To Apidra 100 Μονάδες/ml, ενέσιμο διάλυμα σε ένα φιαλίδιο των 10 ml είναι ένα διαυγές, άχρωμο, υδατικό διάλυμα χωρίς
Rev 02 - Final ΟΔΗΓΟΣ ΓΙΑ ΝΑ ΑΡΧΙΣΕΤΕ ΜΕ ΤΟ APIDRA ενέσιμο διάλυμα σε φιαλίδιο των 10 ml To Apidra 100 Μονάδες/ml, ενέσιμο διάλυμα σε ένα φιαλίδιο των 10 ml είναι ένα διαυγές, άχρωμο, υδατικό διάλυμα χωρίς
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ. Nasoxyl 0.1% nasal spray Ξυλομεταζολίνη HCl
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Nasoxyl 0.1% nasal spray Ξυλομεταζολίνη HCl Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης, διότι περιέχει πληροφορίες που είναι σημαντικές για σας.
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ Nasoxyl 0.1% nasal spray Ξυλομεταζολίνη HCl Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης, διότι περιέχει πληροφορίες που είναι σημαντικές για σας.
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία: RELIEF 1.2 Σύνθεση: Δραστική ουσία: Thiocolchicoside Έκδοχα: Lactose monohydrate, Maize starch, Magnesium stearate
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Ονομασία: RELIEF 1.2 Σύνθεση: Δραστική ουσία: Thiocolchicoside Έκδοχα: Lactose monohydrate, Maize starch, Magnesium stearate
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ
 Covexin 8Α ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1. ΟΝΟΜΑ ΚΑΙ ΔΙΕΥΘΥΝΣΗ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ ΚΑΙ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΠΑΡΑΓΩΓΗΣ ΠΟΥ ΕΙΝΑΙ ΥΠΕΥΘΥΝΟΣ ΓΙΑ ΤΗΝ ΑΠΟΔΕΣΜΕΥΣΗ ΠΑΡΤΙΔΩΝ ΣΤΟΝ ΕΟΧ, ΕΦΟΣΟΝ ΕΙΝΑΙ ΔΙΑΦΟΡΕΤΙΚΟΙ
Covexin 8Α ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ 1. ΟΝΟΜΑ ΚΑΙ ΔΙΕΥΘΥΝΣΗ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΚΥΚΛΟΦΟΡΙΑΣ ΚΑΙ ΤΟΥ ΚΑΤΟΧΟΥ ΤΗΣ ΑΔΕΙΑΣ ΠΑΡΑΓΩΓΗΣ ΠΟΥ ΕΙΝΑΙ ΥΠΕΥΘΥΝΟΣ ΓΙΑ ΤΗΝ ΑΠΟΔΕΣΜΕΥΣΗ ΠΑΡΤΙΔΩΝ ΣΤΟΝ ΕΟΧ, ΕΦΟΣΟΝ ΕΙΝΑΙ ΔΙΑΦΟΡΕΤΙΚΟΙ
Ανακούφιση των συμπτωμάτων ήπιας έως μέτριας οστεοαρθρίτιδας των γονάτων.
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ EFFER ACTIV 2.ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε δισκίο περιέχει 1,5 g γλυκοζαμίνης (ως υδροχλωρική γλυκοζαμίνη) Για τον
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΙΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΙΟΝΤΟΣ EFFER ACTIV 2.ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε δισκίο περιέχει 1,5 g γλυκοζαμίνης (ως υδροχλωρική γλυκοζαμίνη) Για τον
Τι είναι το γλαύκωμα;
 Αυτές οι πληροφορίες προορίζονται για γενική πληροφόρηση και ενημέρωση του κοινού και σε καμία περίπτωση δεν μπορούν να αντικαταστήσουν τη συμβουλή ιατρού ή άλλου αρμοδίου επαγγελματία υγείας. Τι είναι
Αυτές οι πληροφορίες προορίζονται για γενική πληροφόρηση και ενημέρωση του κοινού και σε καμία περίπτωση δεν μπορούν να αντικαταστήσουν τη συμβουλή ιατρού ή άλλου αρμοδίου επαγγελματία υγείας. Τι είναι
Written by Δρ Δημήτριος Ν. Γκέλης, Ιατρός, Οδοντίατρος, Ωτορινολαρυγγολόγος, -
 ALTAXA ΠΕΡΙΛΗΨΗ ΤΟΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ α. α)sumatriptan succinate 50mg/δισκίο β). Sumatriptan succinate 100mg/ δισκίο Για τα έκδοχα βλίπε 'Φαρμακευτικά
ALTAXA ΠΕΡΙΛΗΨΗ ΤΟΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ ΠΟΙΟΤΙΚΗ & ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ ΣΕ ΔΡΑΣΤΙΚΑ ΣΥΣΤΑΤΙΚΑ α. α)sumatriptan succinate 50mg/δισκίο β). Sumatriptan succinate 100mg/ δισκίο Για τα έκδοχα βλίπε 'Φαρμακευτικά
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ Afluon nasal spray SPC 13 EMA (GR120306) 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ AFLUON 0,1% w/v ρινικό εκνέφωμα, διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Διάλυμα
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ Afluon nasal spray SPC 13 EMA (GR120306) 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ AFLUON 0,1% w/v ρινικό εκνέφωμα, διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Διάλυμα
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Molaxole κόνις για πόσιμο διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φακελλίσκος περιέχει τις ακόλουθες δραστικές ουσίες:
ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Molaxole κόνις για πόσιμο διάλυμα 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε φακελλίσκος περιέχει τις ακόλουθες δραστικές ουσίες:
Γλαύκωμα. www.ophthalmica.gr IΝΣΤΙΤΟΥΤΟ ΟΦΘΑΛΜΟΛΟΓΙΑΣ ΚΑΙ ΜΙΚΡΟΧΕΙΡΟΥΡΓΙΚΗΣ
 Γλαύκωμα www.ophthalmica.gr IΝΣΤΙΤΟΥΤΟ ΟΦΘΑΛΜΟΛΟΓΙΑΣ ΚΑΙ ΜΙΚΡΟΧΕΙΡΟΥΡΓΙΚΗΣ Τι ακριβώς είναι το γλαύκωμα; Ο όρος γλαύκωμα ορίζει μια ομάδα παθήσεων που τις χαρακτηρίζει μια σταδιακή καταστροφή του οπτικού
Γλαύκωμα www.ophthalmica.gr IΝΣΤΙΤΟΥΤΟ ΟΦΘΑΛΜΟΛΟΓΙΑΣ ΚΑΙ ΜΙΚΡΟΧΕΙΡΟΥΡΓΙΚΗΣ Τι ακριβώς είναι το γλαύκωμα; Ο όρος γλαύκωμα ορίζει μια ομάδα παθήσεων που τις χαρακτηρίζει μια σταδιακή καταστροφή του οπτικού
Το υαλοειδές αφαιρείται, επίσης, εάν έλκει τον αμφιβληστροειδή από τη φυσική του θέση (έλξη αμφιβληστροειδούς).
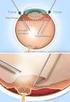 Γράφει: Ευστράτιος Β. Γκοτζαρίδης, Χειρουργός Οφθαλμίατρος Το υαλοειδές είναι μία διαυγής, σαν ζελέ ουσία, που αποτελεί το περιεχόμενο του ματιού, δίνοντάς του δομή και σχήμα πριν από τη γέννηση. Ορισμένα
Γράφει: Ευστράτιος Β. Γκοτζαρίδης, Χειρουργός Οφθαλμίατρος Το υαλοειδές είναι μία διαυγής, σαν ζελέ ουσία, που αποτελεί το περιεχόμενο του ματιού, δίνοντάς του δομή και σχήμα πριν από τη γέννηση. Ορισμένα
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Morphasol 4 mg/ml ενέσιμο διάλυμα για σκύλους και γάτες 2 ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε 1
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ Morphasol 4 mg/ml ενέσιμο διάλυμα για σκύλους και γάτες 2 ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε 1
ραγοειδίτιδα IΝΣΤΙΤΟΥΤΟ ΟΦΘΑΛΜΟΛΟΓΙΑΣ ΚΑΙ ΜΙΚΡΟΧΕΙΡΟΥΡΓΙΚΗΣ
 ραγοειδίτιδα www.ophthalmica.gr IΝΣΤΙΤΟΥΤΟ ΟΦΘΑΛΜΟΛΟΓΙΑΣ ΚΑΙ ΜΙΚΡΟΧΕΙΡΟΥΡΓΙΚΗΣ Τι είναι ο ραγοειδής χιτώνας; Αν σκεφτούμε το μάτι σαν μια σφαιρική κατασκευή που εσωτερικά περιέχει υγρό και εξωτερικά καλύπτεται
ραγοειδίτιδα www.ophthalmica.gr IΝΣΤΙΤΟΥΤΟ ΟΦΘΑΛΜΟΛΟΓΙΑΣ ΚΑΙ ΜΙΚΡΟΧΕΙΡΟΥΡΓΙΚΗΣ Τι είναι ο ραγοειδής χιτώνας; Αν σκεφτούμε το μάτι σαν μια σφαιρική κατασκευή που εσωτερικά περιέχει υγρό και εξωτερικά καλύπτεται
Παράρτημα ΙΙ. Επιστημονικά πορίσματα και λόγοι για την τροποποίηση των όρων των αδειών κυκλοφορίας
 Παράρτημα ΙΙ Επιστημονικά πορίσματα και λόγοι για την τροποποίηση των όρων των αδειών κυκλοφορίας 12 Επιστημονικά πορίσματα και λόγοι για την τροποποίηση των όρων των αδειών κυκλοφορίας Η Συντονιστική
Παράρτημα ΙΙ Επιστημονικά πορίσματα και λόγοι για την τροποποίηση των όρων των αδειών κυκλοφορίας 12 Επιστημονικά πορίσματα και λόγοι για την τροποποίηση των όρων των αδειών κυκλοφορίας Η Συντονιστική
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ. Cetirizine Dihydrochloride
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ DERMIZIN 10 mg/ml Cetirizine Dihydrochloride Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο. - Φυλάξτε
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ: ΠΛΗΡΟΦΟΡΙΕΣ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ DERMIZIN 10 mg/ml Cetirizine Dihydrochloride Διαβάστε προσεκτικά ολόκληρο το φύλλο οδηγιών χρήσης προτού αρχίσετε να παίρνετε αυτό το φάρμακο. - Φυλάξτε
ΠΑΡΑΡΤΗΜΑ I ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΑΡΑΡΤΗΜΑ I ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ JETREA 0,5 mg/0,2 ml πυκνό διάλυμα για παρασκευή ενεσίμου διαλύματος 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε
ΠΑΡΑΡΤΗΜΑ I ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ JETREA 0,5 mg/0,2 ml πυκνό διάλυμα για παρασκευή ενεσίμου διαλύματος 2. ΠΟΙΟΤΙΚΗ ΚΑΙ ΠΟΣΟΤΙΚΗ ΣΥΝΘΕΣΗ Κάθε
Παράρτημα Ι. Επιστημονικά πορίσματα και λόγοι για την αναστολή της άδειας κυκλοφορίας που παρουσιάστηκαν από τον Ευρωπαϊκό Οργανισμό Φαρμάκων
 Παράρτημα Ι Επιστημονικά πορίσματα και λόγοι για την αναστολή της άδειας κυκλοφορίας που παρουσιάστηκαν από τον Ευρωπαϊκό Οργανισμό Φαρμάκων 1 Επιστημονικά πορίσματα Γενική περίληψη της επιστημονικής αξιολόγησης
Παράρτημα Ι Επιστημονικά πορίσματα και λόγοι για την αναστολή της άδειας κυκλοφορίας που παρουσιάστηκαν από τον Ευρωπαϊκό Οργανισμό Φαρμάκων 1 Επιστημονικά πορίσματα Γενική περίληψη της επιστημονικής αξιολόγησης
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ
 ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ CORTAVANCE 0,584 mg/ml διάλυμα σε εκνέφωμα για τοπική εξωτερική χρήση στους σκύλους 2. ΠΟΙΟΤΙΚΗ
ΠΑΡΑΡΤΗΜΑ Ι ΠΕΡΙΛΗΨΗ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ 1 1. ΟΝΟΜΑΣΙΑ ΤΟΥ ΚΤΗΝΙΑΤΡΙΚΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ CORTAVANCE 0,584 mg/ml διάλυμα σε εκνέφωμα για τοπική εξωτερική χρήση στους σκύλους 2. ΠΟΙΟΤΙΚΗ
Γενική περίληψη της επιστημονικής αξιολόγησης του Kytril και των λοιπών εμπορικών ονομασιών του (βλ. Παράρτημα Ι)
 ΠΑΡΑΡΤΗΜΑ ΙΙ ΕΠΙΣΤΗΜΟΝΙΚΑ ΠΟΡΙΣΜΑΤΑ ΚΑΙ ΛΟΓΟΙ ΓΙΑ ΤΗΝ ΤΡΟΠΟΠΟΙΗΣΗ ΤΗΣ ΠΕΡΙΛΗΨΗΣ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ, ΤΗΣ ΕΠΙΣΗΜΑΝΣΗΣ ΚΑΙ ΤΟΥ ΦΥΛΛΟΥ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ ΠΟΥ ΠΑΡΟΥΣΙΑΣΤΗΚΑΝ ΑΠΟ ΤΟΝ ΕΥΡΩΠΑΪΚΟ ΟΡΓΑΝΙΣΜΟ
ΠΑΡΑΡΤΗΜΑ ΙΙ ΕΠΙΣΤΗΜΟΝΙΚΑ ΠΟΡΙΣΜΑΤΑ ΚΑΙ ΛΟΓΟΙ ΓΙΑ ΤΗΝ ΤΡΟΠΟΠΟΙΗΣΗ ΤΗΣ ΠΕΡΙΛΗΨΗΣ ΤΩΝ ΧΑΡΑΚΤΗΡΙΣΤΙΚΩΝ ΤΟΥ ΠΡΟΪΟΝΤΟΣ, ΤΗΣ ΕΠΙΣΗΜΑΝΣΗΣ ΚΑΙ ΤΟΥ ΦΥΛΛΟΥ ΟΔΗΓΙΩΝ ΧΡΗΣΗΣ ΠΟΥ ΠΑΡΟΥΣΙΑΣΤΗΚΑΝ ΑΠΟ ΤΟΝ ΕΥΡΩΠΑΪΚΟ ΟΡΓΑΝΙΣΜΟ
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Oνομασία: CLOPIXOL ΑCUTARD 1.2 Σύνθεση: Δραστική ουσία: Zuclopenthixol acetate (Ζουκλοπενθιξόλη) Έκδοχα: Triglycerides, medium-chain
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟΝ ΧΡΗΣΤΗ 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΠΡΟΪΟΝΤΟΣ 1.1 Oνομασία: CLOPIXOL ΑCUTARD 1.2 Σύνθεση: Δραστική ουσία: Zuclopenthixol acetate (Ζουκλοπενθιξόλη) Έκδοχα: Triglycerides, medium-chain
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ
 ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΙΔΙΟΣΚΕΥΑΣΜΑΤΟΣ 1.1 Ονομασία: LOCERYL ΛΑΚΑ ΟΝΥΧΩΝ 5% Amorolfine 1.2 Σύνθεση Δραστική ουσία: Amorolfine Έκδοχα: Συμπολυμερές μεθακρυλικού οξέος
ΦΥΛΛΟ ΟΔΗΓΙΩΝ ΓΙΑ ΤΟ ΧΡΗΣΤΗ 1. ΠΡΟΣΔΙΟΡΙΣΜΟΣ ΤΟΥ ΦΑΡΜΑΚΕΥΤΙΚΟΥ ΙΔΙΟΣΚΕΥΑΣΜΑΤΟΣ 1.1 Ονομασία: LOCERYL ΛΑΚΑ ΟΝΥΧΩΝ 5% Amorolfine 1.2 Σύνθεση Δραστική ουσία: Amorolfine Έκδοχα: Συμπολυμερές μεθακρυλικού οξέος
